Химические свойства воды. 6 основных типов химических реакций для воды.
Химические свойства воды. 6 основных типов химических реакций для воды. ( хороший обзор Новосибирского Университета)Давайте вспомним все уже известные нам реакции, в которых участвует вода. Для этого вновь напишем уравнения встречавшихся ранее реакций и систематизируем их. Оказывается, вода – весьма активное в химическом отношении вещество.
1) Вода реагирует со многими металлами с выделением водорода:
2Na + 2H2O = H2 + 2NaOH (бурно)
2K + 2H2O = H2 + 2KOH (бурно)
3Fe + 4H2O = 4H2 + Fe3O4 (только при нагревании)
Не все, а только достаточно активные металлы могут участвовать в окислительно-восстановительных реакциях этого типа. Наиболее легко реагируют щелочные и щелочноземельные металлы I и II групп.
Из неметаллов с водой реагируют, например, углерод и его водородное соединение (метан). Эти вещества гораздо менее активны, чем металлы, но все же способны реагировать с водой при высокой температуре:
C + H2O = H2 + CO (при сильном нагревании)
CH4 + 2H2O = 4H2 + CO2 (при сильном нагревании)
2) Электролиз. Вода разлагается на водород и кислород при действии электрического тока. Это также окислительно-восстановительная реакция, где вода является одновременно и окислителем, и восстановителем.
3) Вода реагирует со многими оксидами неметаллов. В отличие от предыдущих, эти реакции не окислительно-восстановительные, а реакции соединения:
|
SO2 |
+ |
H2O |
= |
H2SO3 |
|
сернистая кислота |
|
SO3 |
+ |
H2O |
= |
H2SO4 |
|
серная кислота |
|
CO2 |
+ |
H2O |
= |
H2CO3 |
|
угольная кислота |
4) Некоторые оксиды металлов также могут вступать в реакции соединения с водой. Примеры таких реакций мы уже встречали:
|
CaO |
+ |
H2O |
= |
Ca(OH)2 |
|
гидроксид кальция (гашеная известь) |
Не все оксиды металлов способны реагировать с водой. Часть из них практически не растворима в воде и поэтому с водой не реагирует. Мы уже встречались с такими оксидами. Это ZnO, TiO2, Cr2O3, из которых приготовляют, например, стойкие к воде краски. Оксиды железа также не растворимы в воде и не реагируют с ней.
5) Вода образует многочисленные соединения, в которых ее молекула полностью сохраняется. Это так называемые гидраты. Если гидрат кристаллический, то он называется кристаллогидратом. Например:
|
CuSO4 |
+ |
5 H2O |
= |
CuSO4.5H2O |
|
вещество белого цвета (безводный сульфат меди) |
кристаллогидрат (медный купорос),синие кристаллы |
Приведем другие примеры образования гидратов:
H2SO4 + H2O = H2SO4.H2O (гидрат серной кислоты)
NaOH + H2O = NaOH.H2O (гидрат едкого натра)
Соединения, связывающие воду в гидраты и кристаллогидраты, используют в качестве осушителей. С их помощью, например, удаляют водяные пары из влажного атмосферного воздуха.
6) Фотосинтез . Особая реакция воды– синтез растениями крахмала (C6H10O5)n и других подобных соединений (углеводов), происходящая с выделением кислорода:
6n CO2 + 5n H2O = (C6H10O5)n + 6n O2 (при действии света)
tehtab.ru
Свойства воды — Химические и физические свойства воды
Химические и физические свойства воды в жидком состоянии- термины, определения и комментарии
Строго говоря, в этом материале мы кратко рассмотрим не только химические и физические свойства воды в жидком состоянии, но и свойства присущие ей в общем как таковой.
Более подробно со свойствами воды в твердом состоянии вы можете ознакомиться в статье — СВОЙСТВА ВОДЫ В ТВЕРДОМ СОСТОЯНИИ ( читать → ).
Вода — сверх-значимое вещество для нашей планеты. Без нее на Земле жизнь невозможна, без нее не проходит ни один геологический процесс. Великий ученый и мыслитель Владимир Иванович Вернадский в своих работах писал, что не существует такого компонента, значение которого могло бы «сравниться с ней по влиянию на ход основных, самых грозных геологических процессов». Вода присутствует не только в организме всех живых существ нашей планеты, но и во всех веществах на Земле – в минералах, в горных породах … Изучение уникальных свойств воды постоянно открывает нам все новые и новые тайны, задает нам новые загадки и бросает новые вызовы.
Многие физические и химические свойства воды удивляют и выпадают из общих правил и закономерностей и являются аномальными, так например:
- В соответствии с закономерностями, установленными по принципу подобия, в рамках таких наук как химия и физика, мы могли бы ожидать, что:
- вода будет закипать при минус 70°С, а замерзать при минус 90°С;
- вода будет не капать с кончика крана, а литься тонкой струйкой;
- лед будет тонуть, а не плавать на поверхности;
- в стакане воды не растворилось бы более нескольких крупинок сахара.
- Поверхность воды обладает отрицательным электрическим потенциалом;
- При нагревании от 0°C до 4°C (точнее 3,98°C) вода сжимается;
- Вызывает удивление высокая теплоёмкость жидкой воды;
- …
Вода имеет много и других аномалий, исследование которых вероятно принесет, в ближайшем будущем, новые неожиданные открытия.
Необходимо отметить, что вода в естественных природных условиях может существовать в трех агрегатных состояниях, более подробно, с которыми можно ознакомиться в нашей статье — АГРЕГАТНЫЕ СОСТОЯНИЯ ВОДЫ ( читать → ).
Как уже отмечалось выше, в данном материале мы перечислим основные физические и химические свойства воды и сделаем к некоторым из них краткие комментарии.
Физические свойства воды
ФИЗИЧЕСКИЕ СВОЙСТВА – это свойства, которые проявляются вне химических реакций.
Чистота воды
Чистота воды – зависит от наличия в ней примесей, бактерий, солей тяжелых металлов … , для ознакомления с интерпретацией термина ЧИСТАЯ ВОДА по версии нашего сайта необходимо прочитать статью ЧИСТАЯ ВОДА ( читать → ).
Цвет воды
Цвет воды – зависит от химического состава и механических примесей
Для примера приведем определение «Цвета моря», данное «Большой советской энциклопедией».
Большая советская энциклопедия
Цвет моря. Цвет, воспринимаемый глазом, когда наблюдатель смотрит на поверхность моря, Цвет моря зависит от цвета морской воды, цвета неба, количества и характера облаков, высоты Солнца над горизонтом и др. причин.
Понятие Цвет моря следует отличать от понятия цвет морской воды. Под цветом морской воды понимают цвет, воспринимаемый глазом при отвесном осмотре морской воды над белым фоном. От поверхности моря отражается лишь незначительная часть падающих на неё световых лучей, остальная их часть проникает вглубь, где поглощается и рассеивается молекулами воды, частицами взвешенных веществ и мельчайшими пузырьками газов. Отражённые и выходящие из моря рассеянные лучи и создают Ц. м. Молекулы воды рассеивают сильнее всего синий и зелёные лучи. Взвешенные частицы почти одинаково рассеивают все лучи. Поэтому морская вода с малым количеством взвесей кажется сине-зелёной (цвет открытых частей океанов), а со значительным количеством взвесей — желтовато-зелёной (например, Балтийское море). Теоретическая сторона учения о Ц. м. разработана В. В. Шулейкиным и Ч. В. Раманом.
Большая советская энциклопедия. — М.: Советская энциклопедия. 1969—1978
Запах воды
Запах воды – чистая вода как правило, не имеет запаха.
Прозрачность воды
Прозрачность воды — зависит от растворенных в ней минеральных веществ и содержания механических примесей, органических веществ и коллоидов:
Экологический энциклопедический словарь
ПРОЗРАЧНОСТЬ ВОДЫ — способность воды пропускать свет. Обычно измеряется диском Секки. Зависит в основном от концентрации взвешенных и растворенных в воде органических и неорганических веществ. Может резко снижаться в результате антропогенного загрязнения и эвтрофирования водоемов.
Экологический энциклопедический словарь. — Кишинев И.И. Дедю. 1989
Словарь по гидрогеологии и инженерной геологии
ПРОЗРАЧНОСТЬ ВОДЫ — способность воды пропускать световые лучи. Зависит от толщины слоя воды, проходимого лучами, наличия в ней взвешенных примесей, растворенных веществ и т. п. В воде сильнее поглощаются красные и желтые лучи, глубже проникают фиолетовые. По степени прозрачности, в порядке уменьшения ее, различают воды:
- прозрачные;
- слабо опалесцирующие;
- опалесцирующие;
- слегка мутные;
- мутные;
- сильно мутные.
Словарь по гидрогеологии и инженерной геологии. — М.: Гостоптехиздат. 1961
Вкус воды
Вкус воды – зависит от состава растворенных в ней веществ.
Словарь по гидрогеологии и инженерной геологии
Вкус воды — свойство воды, зависящее от растворенных в ней солей и газов. Имеются таблицы ощутимой на вкус концентрации солей, растворенных в воде (в мг/л), например следующая таблица (по Штаффу).
Словарь по гидрогеологии и инженерной геологии. — М.: Гостоптехиздат. Составитель: А. А. Маккавеев, редактор О. К. Ланге. 1961
Температура воды
Температура плавления воды:
Научно-технический энциклопедический словарь
ТЕМПЕРАТУРА ПЛАВЛЕНИЯ — температура, при которой вещество переходит из ТВЕРДОГО СОСТОЯНИЯ в жидкое. Температура плавления твердого вещества равна температуре замерзания жидкости, например, температура плавления льда, О °С, равна температуре замерзания воды.
Научно-технический энциклопедический словарь.
Температура кипения воды: 99,974°C
Научно-технический энциклопедический словарь
ТЕМПЕРАТУРА КИПЕНИЯ, температура, при которой вещество переходит из одного состояния (фазы) в другое, т. е. из жидкости в пар или газ. Температура кипения возрастает при увеличении внешнего давления и понижается при его уменьшении. Обычно ее измеряют при стандартном давлении в 1 атмосфе
vodamama.com
Физические и химические свойства воды
Формула – H2O. Молярная масса – 18 г/моль. Может существовать в трех агрегатных состояниях – жидком (вода), твердом (лед) и газообразном (водяной пар).
Химические свойства воды
Вода – наиболее распространенный растворитель. В растворе воды существует равновесие, поэтому воду называют амфолитом:
H2O ↔ H+ + OH— ↔ H3O+ + OH—.
Под действием электрического тока вода разлагается на водород и кислород:
H2O = H2 + O2.
При комнатной температуре вода растворяет активные металлы с образованием щелочей, при этом также происходит выделение водорода:
2H2O + 2Na = 2NaOH + H2↑.
Вода способна взаимодействовать с фтором и межгалоидными соединениями, причем во втором случае реакция протекает при пониженных температурах:
2H2O + 2F2 = 4HF + O2↑.
3H2O +IF5 = 5HF + HIO3.
Соли, образованные слабым основанием и слабой кислотой, подвергаются гидролизу при растворении в воде:
Al2S3 + 6H2O = 2Al(OH)3↓ + 3H2S↑.
Вода способна растворять некоторые вещества металлы и неметаллы при нагревании:
4H2O + 3Fe = Fe3O4 + 4H2↑;
H2O + C ↔ CO + H2.
Вода, в присутствии серной кислоты, вступает в реакции взаимодействия (гидратации) с непредельными углеводородами – алкенами с образованием предельных одноатомных спиртов:
CH2 = CH2 + H2O → CH3-CH2-OH.
Физические свойства воды
Вода – прозрачная жидкость (н.у.). Дипольный момент – 1,84 Д (за счет сильного различия электроотрицательностей кислорода и водорода). Вода обладает самым высоким значением удельной теплоемкости среди всех веществ в жидком и твердом агрегатном состояних. Удельная теплота плавления воды – 333,25 кДж/кг (0 С), парообразования – 2250 кДж/кг. Вода способна растворять полярные вещества. Вода обладает высоким поверхностным натяжением и отрицательным электрическим потенциалом поверхности.
Получение воды
Воду получают по реакции нейтрализации, т.е. реакции взаимодействия между кислотами и щелочами:
H2SO4 + 2KOH = K2SO4 + H2O;
HNO3 + NH4OH = NH4NO3 + H2O;
2CH3COOH + Ba(OH)2 = (CH3COO)2Ba + H2O.
Один из способов получения воды – восстановление металлов водородом из их оксидов:
CuO + H2 = Cu + H2O.
Примеры решения задач
Химические свойства воды
Из химических свойств воды особенно важны способность её молекул диссоциировать (распадаться) на ионы и способность растворять вещества разной химической природы.
Роль воды как главного и универсального растворителя определяется прежде всего полярностью её молекул и, как следствие, её чрезвычайно высокой диэлектрической проницаемостью. Разноимённые электрические заряды, и в частности ионы, притягиваются друг к другу в воде в 80 раз слабее, чем притягивались бы в воздухе. Силы взаимного притяжения между молекулами или атомами погружённого в воду тела также слабее, чем в воздухе. Тепловому движению в этом случае легче разбить молекулы. Оттого и происходит растворение, в том числе многих труднорастворимых веществ: капля камень точит.
Лишь в незначительной степени протекает электролитическая диссоциация (автодиссоциация воды) по схеме:
Н2О Н+ + ОН—
Однако, приведённое уравнение условное: не может существовать в водной среде лишённый электронной оболочки протон Н+. Он сразу гидратируется водой до катионов оксония Н3О+. Однако для простоты записи обычно используется обозначение Н+.
По Бренстенду такая реакция называется автопротолизом воды:
Н2О + Н2О Н3О+ + ОН—
Электролитическая диссоциация воды – причина гидролиза солей слабых кислот и оснований. Степень электролитической диссоциации заметно возрастает при повышении температуры.
Образование воды из элементов по реакции:
-286 кДж/моль для жидкой воды
При низких температурах в отсутствии катализаторов происходит крайне медленно, но скорость реакции резко возрастает при повышении температуры, и при 5500 С она происходит со взрывом. При понижении давления и повышении температуры равновесие сдвигается влево.
Под действием ультрафиолетового излучения происходит фотодиссоциация воды на ионы Н+ и ОН—.
Вода окисляется атомарным кислородом:
Н2О + О Н2О2
При взаимодействии с F2 образуется НF, а также О2 ;О3 ; Н2О2 ; F2О и другие соединения. С остальными галогенами при низких температурах вода реагирует с образованием смеси кислот Н Гал. и Н Гал. О.
При обычных условиях с водой взаимодействует до половины растворённого в ней СI2 и значительно меньшие количества Br2 и J2. При повышенных температурах СI2 и Br2 разлагают воду с образованием Н Гал. и О2.
При пропускании паров воды через раскалённый уголь она разлагается и образуется так называемый водяной газ:
Н2О + С СО + Н2
При повышенной температуре в присутствии катализатора вода реагирует с СО; СН4 и другими углеводородами, например:
Н2О + СО СО2 + Н2
Н2О + СН4СО + 3Н2
Эти реакции используют для промышленного получения водорода.
Фосфор при нагревании с водой под давлением в присутствии катализатора окисляется в метафосфорную кислоту:
6Н2О + 3Р 2НРО3 + 5Н2
Вода взаимодействует со многими металлами с образованием Н2 и соответствующего гидроксида. Со щелочными и щелочно-земельными металлами (кроме Мg) эта реакция протекает уже при комнатной температуре. Менее активные металлы разлагают воду при повышенной температуре, например, Мg и Zn – выше 1000 С; Fe – выше 6000С :
2Fe + 3H2O Fe2O 3 + 3H2
При взаимодействии с водой многих оксидов образуются кислоты или основания.
Вода может служить катализатором, например, щелочные металлы и водород реагируют с CI2 только в присутствии следов воды.
Иногда вода – каталитический яд, например, для железного катализатора при синтезе NH3.
Способность молекул воды образовывать трёхмерные сетки водородных связей позволяет ей давать с инертными газами, углеводородами, СО2 , CI2 , (CH2)2O , CHCI3 и многими другими веществами газовые гидраты.
studfiles.net
Урок 28. Химические свойства воды – HIMI4KA
В уроке 28 «Химические свойства воды» из курса «Химия для чайников» узнаем о взаимодействии воды с различными веществами.

При обычных условиях вода является достаточно активным веществом по отношению к другим веществам. Это означает, что со многими из них она вступает в химические реакции.
Взаимодействие с оксидами неметаллов
Если струю газообразного оксида углерода(IV) CO2 (углекислого газа) направить в воду, то часть его растворится в ней (рис. 109).

При этом в растворе протекает химическая реакция соединения, в результате которой образуется новое вещество — угольная кислота H2CO3:
На заметку: Собирая углекислый газ над водой, Дж. Пристли обнаружил, что часть газа растворяется в воде и придает ей приятный терпкий вкус. По сути дела, Пристли впервые получил напиток типа газированной, или содовой, воды.
Реакция соединения происходит также, если к воде прибавить твердый оксид фосфора(V) P2O5. При этом протекает химическая реакция с образованием фосфорной кислоты H3PO4 (рис. 110):

Испытаем растворы, полученные при взаимодействии CO2 и P2O5 с водой, индикатором метиловым оранжевым. Для этого прибавим по 1—2 капли раствора индикатора к полученным растворам. Цвет индикатора изменится с оранжевого на красный, что говорит о присутствии кислот в растворах. Значит, при взаимодействии CO2 и P2O5 с водой действительно образовались кислоты H2CO3 и H3PO4.
Оксиды, подобные CO2 и P2O5, которые при взаимодействии с водой образуют кислоты, относят к кислотным оксидам.
Кислотные оксиды — это оксиды, которым соответствуют кислоты.
Некоторые из кислотных оксидов и соответствующих им кислот приведены в таблице 11. Обратите внимание, что это оксиды элементов неметаллов. Как правило, оксиды неметаллов являются кислотными оксидами.
Взаимодействие с оксидами металлов
С оксидами металлов вода реагирует иначе, чем с оксидами неметаллов.
Исследуем взаимодействие оксида кальция CaO с водой. Для этого поместим в стакан с водой небольшое количество CaO и тщательно перемешаем. При этом протекает химическая реакция:
в результате которой образуется новое вещество Ca(OH)2, относящееся к классу оснований. Таким же образом реагируют с водой оксиды лития, натрия. При этом также образуются основания, например:
Подробнее с основаниями вы познакомитесь в следующем уроке. Оксиды металлов, которым соответствуют основания, называют основными оксидами.
Основные оксиды — это оксиды, которым соответствуют основания.
В таблице 12 приведены формулы некоторых основных оксидов и соответствующих им оснований. Заметьте, что, в отличие от кислотных оксидов, в состав основных оксидов входят атомы металлов. Большинство оксидов металлов — это основные оксиды.
Несмотря на то что каждому основному оксиду соответствует основание, не все основные оксиды взаимодействуют с водой, подобно CaO, образуя основания.
Взаимодействие с металлами
При обычных условиях активные металлы (K, Na, Ca, Ba и др.) бурно реагируют с водой:
В этих реакциях выделяется водород и образуются растворимые в воде основания.
Как химически активное вещество вода вступает в реакции со многими другими веществами, но об этом вы узнаете при дальнейшем изучении химии.
Краткие выводы урока:
- Вода — химически активное вещество. Она вступает в реакции с кислотными и основными оксидами, активными металлами.
- При взаимодействии воды с большинством кислотных оксидов образуются соответствующие кислоты.
- Некоторые основные оксиды при реакции с водой образуют растворимые основания.
- При обычных условиях вода реагирует с наиболее активными металлами. При этом образуются растворимые основания и водород.
Надеюсь урок 28 «Химические свойства воды» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
himi4ka.ru
Урок 27. Состав и физические свойства воды – HIMI4KA
В уроке 27 «Состав и физические свойства воды» из курса «Химия для чайников» узнаем, что из себя представляет вода, выясним её состав, а также физические свойства.

Наиболее распространенным оксидом на Земле является оксид водорода H2O, или вода. Без воды, как и без кислорода, невозможна жизнь человека, животных и растений.
Вода — единственное вещество, существующее на Земле одновременно в трех агрегатных состояниях: жидком, твердом и газообразном. Она является основным компонентом морей и океанов, ледников и айсбергов, облаков и тумана.
Около 70 % поверхности Земли покрыто океанами, морями, реками и озерами — природными хранилищами воды. Из космоса толстый слой воды имеет голубой цвет (рис. 104), вот почему нашу планету называют голубой. Вода входит в состав всех живых организмов, а также очень многих минералов.

Состав и строение воды
Как вы уже знаете, молекула воды состоит из трех атомов — двух атомов водорода и одного атома кислорода (рис. 105). Относительная молекулярная масса воды равна:

Следовательно, молярная масса воды равна:
Вода — это вещество с молекулярным строением. В твердом (рис. 106) и жидком агрегатных состояниях молекулы воды прочно связаны друг с другом. Этим во многом объясняется целый ряд удивительных физических свойств воды.

Физические свойства воды
При комнатных условиях вода представляет собой жидкость без вкуса и запаха. В тонком слое вода не имеет цвета. Однако при толщине более 2 м она имеет голубой цвет. Совершенно чистая вода очень плохо проводит электрический ток.
На заметку: По тому, как проводит электрический ток вода, можно судить о ее чистоте — чем ниже электропроводность, тем чище вода.
У большинства веществ в твердом состоянии плотность выше, чем в жидком. В отличие от них вода в твердом агрегатном состоянии (лед) имеет более низкую плотность, чем в жидком. При 0 °С плотность льда равна примерно 0,92 г/см3, а плотность жидкой воды — примерно 1,00 г/см3. Это означает, что лед легче воды, поэтому он не тонет в ней (рис. 107). Такая особенность воды объясняет, почему водоемы начинают замерзать не со дна, а с поверхности и очень редко промерзают до самого дна. Это защищает живые организмы, обитающие в реках и морях, от гибели.
У воды высокая теплоемкость, поэтому она медленно нагревается, но и медленно остывает. Это позволяет морям и океанам накапливать тепло летом (и днем) и высвобождать его зимой (и ночью), что предотвращает резкие колебания температуры воздуха на нашей планете в течение года (и суток). Моря и океаны служат своеобразными аккумуляторами тепла на нашей планете.

При нормальном давлении (101,3 кПа) температура кипения воды равна 100 °С. При понижении давления температура кипения воды понижается. Например, в горах на высоте около 5000 м давление существенно ниже нормального (примерно в два раза), поэтому вода закипает в этих условиях при температуре около 84 °С. Понятно, что варить продукты до готовности в горах необходимо более длительное время. И наоборот, в скороварке, где создается высокое давление, вода закипает при температуре выше 100 °С, что позволяет быстрее приготавливать пищу.
Вода как растворитель
С совершенно чистой водой, не содержащей никаких других веществ, большинство людей никогда не встречается. Такая вода используется только в специальных целях.
Почти все жидкости, с которыми мы сталкиваемся в повседневной жизни и деятельности, представляют собой растворы различных веществ.
Раствор — это однородная смесь двух и более веществ.
Одно из веществ, входящих в состав раствора, называется растворителем, а остальные — растворенными веществами. Очень часто растворителем является вода. Вода может растворять твердые, жидкие и газообразные вещества.
Все природные воды содержат растворенные соли. Их легко обнаружить экспериментально, выпарив воду на часовом стекле. Кроме солей, вода может растворять различные газы. Их присутствие (правда, не всегда) можно обнаружить экспериментально. Например, поместив пробирку с холодной водой из-под крана в теплое место, через некоторое время можно заметить у стенок пробирки пузырьки. Это растворенные газы (преимущественно кислород) выделяются из раствора при его нагревании до комнатной температуры (рис. 108).

Многие жидкости также хорошо растворимы в воде. Например, серная кислота и спирт неограниченно растворяются в воде. В таком случае говорят, что вещество смешивается с водой в любых соотношениях. Из-за хорошей растворимости многих веществ в воде ее иногда называют универсальным растворителем.
Краткие выводы урока:
- Вода не имеет вкуса, цвета (в тонком слое) и запаха, кипит при 100 °С, а переходит в твердое состояние при 0 °С.
- Плотность твердой воды меньше, чем жидкой.
- Раствор — это однородная смесь двух и более веществ.
- Вода является универсальным растворителем — она хорошо растворяет многие твердые, жидкие и газообразные вещества.
Надеюсь урок 27 «Состав и физические свойства воды» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
himi4ka.ru
Вода и ее свойства физические и химические. Структура воды :: SYL.ru
Самое важное, уникальное по свойствам и составу вещество нашей планеты — это, конечно, вода. Ведь именно благодаря ей на Земле жизнь есть, в то время как на других известных сегодня объектах Солнечной системы ее нет. Твердая, жидкая, в виде пара — она нужна и важна любая. Вода и ее свойства составляют предмет изучения целой научной дисциплины — гидрологии.
Количество воды на планете
Если рассматривать показатель количества данного оксида во всех агрегатных состояниях, то его на планете около 75% от общей массы. При этом следует учитывать связанную воду в органических соединениях, живых существах, минералах и прочих элементах.

Если учитывать только жидкое и твердое состояние воды, показатель падет до 70,8%. Рассмотрим, как распределяются эти проценты, где содержится рассматриваемое вещество.
- Соленой воды в океанах и морях, солончаковых озерах на Земле 360 млн км2.
- Пресная вода распределена неравномерно: ее в ледниках Гренландии, Арктики, Антарктиды заковано во льды 16,3 млн км2.
- В пресных реках, болотах и озерах сосредоточено 5,3 млн км2 оксида водорода.
- Подземные воды составляют 100 млн м3.
Именно поэтому космонавтам из далекого космического пространства видно Землю в форме шара голубого цвета с редкими вкраплениями суши. Вода и ее свойства, знание особенностей строения являются важными элементами науки. К тому же, в последнее время человечество начинает испытывать явную нехватку пресной воды. Может быть, такие знания помогут в решении данной проблемы.
Состав воды и строение молекулы
Если рассмотреть эти показатели, то сразу станут понятны и свойства, которые проявляет это удивительное вещество. Так, молекула воды состоит из двух атомов водорода и одного атома кислорода, поэтому имеет эмпирическую формулу Н2О. Кроме того, при построении самой молекулы большую роль играют электроны обоих элементов. Посмотрим, что собой представляют структура воды и ее свойства.

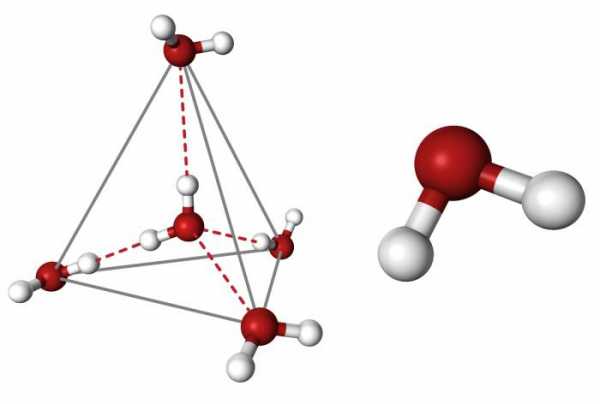
Очевидно, что каждая молекула ориентирована вокруг другой, и все вместе они формируют общую кристаллическую решетку. Интересно то, что оксид построен в форме тетраэдра — атом кислорода в центре, а две пары электронов его и два атома водорода вокруг асимметрично. Если провести через центры ядер атомов линии и соединить их, то получится именно тетраэдрическая геометрическая форма.
Угол между центром атома кислорода и ядрами водородов составляет 104,5 0С. Длина связи О-Н = 0,0957 нм. Наличие электронных пар кислорода, а также его большее в сравнении с водородами сродство к электрону обеспечивают формирование в молекуле отрицательно заряженного поля. В противовес ему ядра водородов образуют положительно заряженную часть соединения. Таким образом, выходит, что молекула воды — диполь. Это определяет то, какой может быть вода, и ее физические свойства также зависят от строения молекулы. Для живых существ эти особенности играют жизненно важную роль.
Основные физические свойства
К таковым принято относить кристаллическую решетку, температуры кипения и плавления, особенные индивидуальные характеристики. Все их и рассмотрим.
- Строение кристаллической решетки оксида водорода зависит от агрегатного состояния. Оно может быть твердым — лед, жидким — основная вода при обычных условиях, газообразным — пар при повышении температуры воды свыше 100 0С. Красивые узорные кристаллы формирует лед. Решетка в целом рыхлая, но соединение очень прочное, плотность низкая. Видеть ее можно на примере снежинок или морозных узоров на стеклах. У обычной воды решетка не имеет постоянной формы, она изменяется и переходит из одного состояния в другое.
- Молекула воды в космическом пространстве имеет правильную форму шара. Однако под действием земной силы тяжести она искажается и в жидком состоянии принимает форму сосуда.
- То, что по структуре оксид водорода — диполь, обуславливает следующие свойства: высокая теплопроводность и теплоемкость, которая прослеживается в быстром нагревании и долгом остывании вещества, способность ориентировать вокруг себя как ионы, так и отдельные электроны, соединения. Это делает воду универсальным растворителем (как полярным, так и нейтральным).
- Состав воды и строение молекулы объясняют способность этого соединения образовывать множественные водородные связи, в том числе с другими соединениями, имеющими неподеленные электронные пары (аммиак, спирт и прочие).
- Температура кипения жидкой воды — 1000С, кристаллизация наступает при +40С. Ниже этого показателя — лед. Если же увеличивать давление, то температура кипения воды резко возрастет. Так, при высоких атмосферах в ней можно растопить свинец, но она при этом даже не закипит (свыше 3000С).
- Свойства воды весьма значимы для живых существ. Например, одно из самых важных — поверхностное натяжение. Это формирование тончайшей защитной пленки на поверхности оксида водорода. Речь идет о воде в жидком состоянии. Эту пленку разорвать механическим воздействием очень сложно. Учеными установлено, что понадобится сила, равная весу в 100 тонн. Как ее заметить? Пленка очевидна, когда вода капает из крана медленно. Видно, что она словно в какой-то оболочке, которая растягивается до определенного предела и веса и отрывается в виде круглой капельки, слегка искаженной силой тяжести. Благодаря поверхностному натяжению многие предметы могут находиться на поверхности воды. Насекомые, имеющие особые приспособления, могут свободно передвигаться по ней.
- Вода и ее свойства аномальны и уникальны. По органолептическим показателям данное соединение — бесцветная жидкость без вкуса и запаха. То, что мы называем вкусом воды, — это растворенные в ней минералы и другие компоненты.
- Электропроводность оксида водорода в жидком состоянии зависит от того, сколько и каких солей в нем растворены. Дистиллированная вода, не содержащая никаких примесей, электрический ток не проводит.
Лед — это особое состояние воды. В структуре этого ее состояния молекулы связаны друг с другом водородными связями и формируют красивую кристаллическую решетку. Но она достаточно неустойчива и легко может расколоться, растаять, то есть деформироваться. Между молекулами сохраняется множество пустот, размеры которых превышают размеры самих частиц. Благодаря этому плотность льда меньше, чем жидкого оксида водорода.

Это имеет большое значение для рек, озер и прочих пресных водоемов. Ведь в зимний период вода в них не замерзает полностью, а лишь покрывается плотной коркой более легкого льда, всплывающего наверх. Если бы данное свойство не было характерно для твердого состояния оксида водорода, то водоемы промерзали бы насквозь. Жизнь под водой была бы невозможна.
Кроме того, твердое состояние воды имеет большое значение как источник огромного количества питьевых пресных запасов. Это ледники.
Особенным свойством воды можно назвать явление тройной точки. Это такое состояние, при котором лед, пар и жидкость могут существовать одновременно. Для этого требуются такие условия, как:
- высокое давление — 610 Па;
- температура 0,010С.
Показатель прозрачности воды варьируется в зависимости от посторонних примесей. Жидкость может быть полностью прозрачной, опалесцентной, мутной. Поглощаются волны желтого и красного цветов, глубоко проникают лучи фиолетовые.

Химические свойства
Вода и ее свойства — важный инструмент в понимании многих процессов жизнедеятельности. Поэтому они изучены очень хорошо. Так, гидрохимию интересуют вода и ее химические свойства. Среди них можно назвать следующие:
- Жесткость. Это такое свойство, которое объясняется наличием солей кальция и магния, их ионов в растворе. Подразделяется на постоянную (соли названных металлов: хлоридов, сульфатов, сульфитов, нитратов), временную (гидрокарбонаты), которая устраняется кипячением. В России воду перед использованием смягчают химическим путем для лучшего качества.
- Минерализация. Свойство, основанное на дипольном моменте оксида водорода. Благодаря его наличию молекулы способны присоединять к себе множество других веществ, ионов и удерживать их. Так формируются ассоциаты, клатраты и прочие объединения.
- Окислительно-восстановительные свойства. Как универсальный растворитель, катализатор, ассоциат, вода способна взаимодействовать с множеством простых и сложных соединений. С одними она выступает в роли окислителя, с другими — наоборот. Как восстановитель реагирует с галогенами, солями, некоторыми менее активными металлами, с многими органическими веществами. Последние превращения изучает органическая химия. Вода и ее свойства, в частности, химические, показывают, насколько она универсальна и уникальна. Как окислитель она вступает в реакции с активными металлами, некоторыми бинарными солями, многими органическими соединениями, углеродом, метаном. Вообще химические реакции с участием данного вещества нуждаются в подборе определенных условий. Именно от них и будет зависеть исход реакции.
- Биохимические свойства. Вода является неотъемлемой частью всех биохимических процессов организма, являясь растворителем, катализатором и средой.
- Взаимодействие с газами с образованием клатратов. Обычная жидкая вода может поглощать даже неактивные химически газы и располагать их внутри полостей между молекулами внутренней структуры. Такие соединения принято называть клатратами.
- Со многими металлами оксид водорода формирует кристаллогидраты, в которые он включен в неизменном виде. Например, медный купорос (CuSO4*5H2O), а также обычные гидраты (NaOH*H2O и другие).
- Для воды характерны реакции соединения, при которых происходит образование новых классов веществ (кислот, щелочей, оснований). Они не являются окислительно-восстановительными.
- Электролиз. Под действием электрического тока молекула разлагается на составные газы — водород и кислород. Один из способов получения их в лаборатории и промышленности.
С точки зрения теории Льюиса вода — это слабая кислота и слабое основание одновременно (амфолит). То есть можно сказать о некоей амфотерности в химических свойствах.

Вода и ее полезные свойства для живых существ
Сложно переоценить то значение, которое имеет оксид водорода для всего живого. Ведь вода и есть сам источник жизни. Известно, что без нее человек не смог бы прожить и недели. Вода, ее свойства и значение просто колоссальны.
- Это универсальный, то есть способный растворять и органические, и неорганические соединения, растворитель, действующий в живых системах. Именно поэтому вода — источник и среда для протекания всех каталитических биохимических преобразований, с формированием сложных жизненно важных комплексных соединений.
- Способность образовывать водородные связи делает данное вещество универсальным в выдерживании температур без изменения агрегатного состояния. Если бы это было не так, то при малейшем снижении градусов она превращалась бы в лед внутри живых существ, вызывая гибель клеток.
- Для человека вода — источник всех основных бытовых благ и нужд: приготовление пищи, стирка, уборка, принятие ванны, купание и плавание и прочее.
- Промышленные заводы (химические, текстильные, машиностроительные, пищевые, нефтеперерабатывающие и другие) не сумели бы осуществлять свою работу без участия оксида водорода.
- Издревле считалось, что вода — это источник здоровья. Она применялась и применяется сегодня как лечебное вещество.
- Растения используют ее как основной источник питания, за счет чего они продуцируют кислород — газ, благодаря которому существует жизнь на нашей планете.
Можно назвать еще десятки причин того, почему вода — это самое широко распространенное, важное и необходимое вещество для всех живых и искусственно созданных человеком объектов. Мы привели только самые очевидные, главные.

Гидрологический цикл воды
Иными словами, это ее круговорот в природе. Очень важный процесс, позволяющий постоянно пополнять исчезающие запасы воды. Как он происходит?
Основных участников трое: подземные (или грунтовые) воды, поверхностные воды и Мировой океан. Важна также и атмосфера, конденсирующая и выдающая осадки. Также активными участниками процесса являются растения (в основном деревья), способные поглощать огромное количество воды в сутки.
Итак, процесс происходит следующим образом. Грунтовые воды заполняют подземные капилляры и стекаются к поверхности и Мировому океану. Затем поверхностные воды поглощаются растениями и транспирируются в окружающую среду. Также происходит испарение с огромных площадей океанов, морей, рек, озер и прочих водоемов. Попав в атмосферу, вода что делает? Конденсируется и проливается обратно в виде осадков (дождь, снег, град).
Если бы не происходили эти процессы, то запасы воды, особенно пресной, давно бы уже закончились. Именно поэтому охране и нормальному гидрологическому циклу уделяется людьми большое внимание.
Понятие о тяжелой воде
В природе оксид водорода существует в виде смеси изотопологов. Это связано с тем, что водород формирует три вида изотопа: протий 1Н, дейтерий 2Н, тритий 3Н. Кислород, в свою очередь, также не отстает и образует три устойчивые формы: 16О, 17О, 18О. Именно благодаря этому существует не просто обычная протиевая вода состава Н2О (1Н и 16О), но еще и дейтериевая, и тритиевая.

При этом устойчива по структуре и форме именно дейтериевая (2Н), которая включается в состав практически всех природных вод, но в малом количестве. Именно ее называют тяжелой. Она несколько отличается от обычной или легкой по всем показателям.
Тяжелая вода и ее свойства характеризуются несколькими пунктами.
- Кристаллизуется при температуре 3,82 0С.
- Кипение наблюдается при 101,42 0С.
- Плотность составляет 1,1059 г/см3.
- Как растворитель в несколько раз хуже легкой воды.
- Имеет химическую формулу D2O.
При проведении опытов, показывающих влияние подобной воды на живые системы, было установлено, что жить в ней способны лишь некоторые виды бактерий. Для приспособления и акклиматизации колониям потребовалось время. Но, приспособившись, они полностью восстановили все жизненно важные функции (размножение, питание). Кроме того, стали очень устойчивы к воздействию радиоактивного излучения. Опыты на лягушках и рыбах положительного результата не дали.
Современные области применения дейтерия и образованной им тяжелой воды — атомная и ядерная энергетика. Получить в лабораторных условиях такую воду можно при помощи электролиза обычной — она образуется как побочный продукт. Сам дейтерий формируется при многократных перегонках водорода в специальных устройствах. Применение его основано на способности замедлять нейтронные синтезы и протонные реакции. Именно тяжелая вода и изотопы водорода — основа для создания ядерной и водородной бомбы.
Опыты на применении дейтериевой воды людьми в небольших количествах показали, что задерживается она недолго — полный вывод наблюдается через две недели. Употреблять ее в качестве источника влаги для жизни нельзя, однако техническое значение просто огромно.
Талая вода и ее применение
Свойства такой воды издревле были определены людьми как целебные. Давно было замечено, что при таянии снега животные стараются напиться водой из образовавшихся лужиц. Позже были тщательно исследованы ее структура и биологическое воздействие на организм человека.

Талая вода, ее признаки и свойства находятся посередине между обычной легкой и льдом. Изнутри она образована не просто молекулами, а набором кластеров, сформированных кристаллами и газом. То есть внутри пустот между структурными частями кристалла находятся водород и кислород. По общему виду строение талой воды сходно со строением льда — сохраняется структурность. Физические свойства такого оксида водорода незначительно меняются в сравнении с обычным. Однако биологическое воздействие на организм отличное.
При замораживании воды первой фракцией превращается в лед более тяжелая часть — это дейтериевые изотопы, соли и примеси. Поэтому эту сердцевину следует удалять. А вот остальная часть — чистая, структурированная и полезная вода. Каково воздействие на организм? Учеными Донецкого НИИ были названы следующие виды улучшений:
- Ускорение восстановительных процессов.
- Укрепление иммунитета.
- У детей после ингаляций такой водой происходит восстановление и излечение простудных заболеваний, проходит кашель, насморк и прочее.
- Улучшается дыхание, состояние гортани и слизистых оболочек.
- Общее самочувствие человека, активность повышаются.
Сегодня существует ряд сторонников лечения именно талой водой, которые пишут свои положительные отзывы. Однако есть ученые, в том числе медики, которые эти взгляды не поддерживают. Они считают, что вреда от такой воды не будет, но и пользы мало.
Энергетика
Почему свойства воды могут изменяться и восстанавливаться при переходе в разные агрегатные состояния? Ответ на этот вопрос следующий: у данного соединения существует своя информационная память, которая записывает все изменения и приводит к восстановлению структуры и свойств в нужное время. Биоэнергетическое поле, через которое проходит часть воды (та, что поступает из космоса), несет в себе мощный заряд энергии. Эту закономерность часто используют при лечении. Однако с медицинской точки зрения не каждая вода способна оказать благоприятный эффект, в том числе и информационный.
Структурированная вода — что это?
Это такая вода, которая имеет несколько иное строение молекул, расположение кристаллических решеток (такое, которое наблюдается у льда), но это все же жидкость (талая также относится к этому типу). В этом случае состав воды и ее свойства с научной точки зрения не отличаются от тех, что характерны для обычного оксида водорода. Поэтому структурированная вода не может иметь такого широкого лечебного эффекта, который ей приписывают эзотерики и сторонники нетрадиционной медицины.
www.syl.ru

