Как устроена батарейка? Принципы работы батарейки
Всего просмотров: 7 631Просмотров за сутки: 0Кто изобрел батарейку?
Если верить археологам, то первые батарейки появились еще 2000 лет назад. Во время раскопок в Ираке нашли глиняную вазу, залитую битумом, в который были вделаны медный и железный стержень. Действительно ли это использовалось в качестве источника электричества, трудно сказать — это всего лишь предположения.
Первой современной батарейкой по праву можно назвать «Вольтов столб» — устройство, созданное итальянским физиком Алессандро Вольта в 1800 году.
 Алессандро Вольта
Алессандро Вольта«Вольтов столб» представлял собой стопку из пластин разных металлов — цинковых и медных. Между ними клалась ткань, смоченная в кислоте. Химическая реакция между элементами «Вольтова столба» создавала электричество.
Вольтов столбЕго работа основывалась на предположениях Луиджи Гальвани, который проводил опыты с лягушкой, подводя к ее лапке металлические полоски.
 Луиджи Гальвани
Луиджи ГальваниОднако, Л. Гальвани сделал неправильные выводы, решив, что само животное обладает электричеством, назвав это «животным электричеством». А. Вольта правильно понял, что разряд возникал из-за того, что лапка, находившаяся между двумя полосками металла, была влажной и служила в качестве проводника.
По имени Л. Гальвани «Вольтов столб» и другие источники электричества подобного типа получили название «Элемента Гальвани» или «Гальванического элемента». Это, на самом деле, более правильное название для таких устройств, так как батарейка — это батарея, т.е. серия гальванических элементов, соединенных между собой. А единицу напряжения, которую давал гальванический элемент, назвали «вольтом» в честь Алессандро Вольта.
Принцип работы батарейки
Во многом принцип работы батарейки тот же, что и в изобретении Вольта, несмотря на технологический прогресс в их изготовлении. Любая батарейка устроена схожим образом, в ней обязательны три элемента, между которыми происходит химическая реакция, в результате которой возникает электричество: электроды — анод, катод, и электролит.
 Устройство батарейки
Устройство батарейкиВсе эти элементы присутствовали изначально и в «Вольтовом столбе». В качестве анода, который является источником электронов, выступает чаще всего цинк. Электролит — как правило, специальное вещество (соль, щелочь), через которое осуществляется взаимодействие электродов между собой. Анод обозначается как «-» (минус), а катод — как «+» (плюс).
Какие бывают батарейки?
Батарейки бывают, в основном, солевыми и щелочными. Жидкие электролиты в них не используются, их определенным образом сгущают, например, при помощи крахмала.
Солевые батарейки, изобретенные в 1865 году — наиболее дешевые в изготовлении, для их производства используют уголь, цинк и хлорид аммония (в качестве электролита). Помимо простоты изготовления и дешевизны, имеют такие недостатки, как окисление, засоливание цинковой оболочки, что приводит солевую батарейку в негодность.
Щелочные батарейки имеют маркировку Alkaline, хранятся они дольше и дают более стабильное напряжение.
 Щелочные батарейки
Щелочные батарейкиВ принципе, это те же солевые батарейки, однако, разница между солевыми и щелочными батарейками заключается в том, что элементы в них расположены в обратном порядке, а цинк находится в порошкообразном состоянии, что увеличивает контакт элементов батареи между собой, делает их более надежными. Щелочные батарейки имеют гораздо больший объем заряда, что позволяет их использовать в энергоемких приборах (цифровых фотоаппаратах, фонариках, электронные игрушки с электродвигателями и т.п.). Они долговечны, лучше справляются с работой при низких температурах.
Наиболее современны литиевые батарейки (литий входит в состав анода), которые долговечны и безопасны в работе однако, дороже в производстве.
 Литиевые батарейки
Литиевые батарейкиК их преимуществам по сравнению с щелочными можно отнести возможность создавать максимально плоские батареи, изготавливать батареи с большим количеством вариантов напряжения, долговечность — в некоторых приборах они могут работать до 15 лет! Их используют в наручных часах, калькуляторах, памяти системной платы компьютера и других приборах.
Проблема всех батареек — необратимость химических реакций. При использовании или с течением времени анод разрушается, либо покрывается продуктами окисления и перестает работать. В таких случаях мы говорим, что батарейка села. Но прогресс не стоит на месте — оказалось, что соединив определенным образом вещества, входящие в состав батареи, можно, пропустив ток через нее, вернуть в прежнее состояние. Такие батареи назвали аккумуляторами — работа батареи в них восстанавливается посредством пропускания электричества в обратном направлении, от катода к аноду. А сам процесс мы все знаем, как «зарядку», т.е. батарея «заряжается». Обычные батареи, рассмотренные выше, заряжать, конечно, нельзя, они для этого не приспособлены — это может привести к их течи или взрыву.
daju-spravku.ru
какие процессы скрыты под оболочкой
 Батарейки являются наиболее распространенным источником питания. Современный мир не представляет себя без различной электроники, для них необходима электроэнергия. Не всегда получается применять обычные сетевые источники, для этого и нужны гальванические элементы. Глядя на них наверняка каждый задавался вопросом из чего состоит батарейка и как она работает.
Батарейки являются наиболее распространенным источником питания. Современный мир не представляет себя без различной электроники, для них необходима электроэнергия. Не всегда получается применять обычные сетевые источники, для этого и нужны гальванические элементы. Глядя на них наверняка каждый задавался вопросом из чего состоит батарейка и как она работает.Что такое батарейка
Обыкновенная батарейка представляет собой электрический источник питания на основе химических реакций. При взаимодействии двух металлических электродов в жидком или твердом электролите происходит выработка энергии в результате взаимодействия элементов. Первая батарейка была изобретена более 2000 лет тому назад, при реакции меди и железа в уксусе вырабатывалось напряжение 1 В.
Важно! Одиночные гальванические элементы не подлежат восстановлению заряда.
Разновидности
По форме и размерам согласно мировым стандартам элементы питания разделяются на такие виды:
- АА- пальчиковая;
- ААА- мизинчиковая;
- АААА;
- С- дюймовочка;
- D- бочка;
- квадратная;
- РР3- крона;
- Источники питания миниатюрных размеров.
В настоящее время существует большое количество разнообразных источников питания. Между собой они отличаются материалами, применяемыми для изготовления электродов и электролита. Среди многочисленных батареек выделяют несколько основных видов:
- солевые;
- щелочные;
- ртутные;
- серебряные;
- литиевые.
Солевые
Такие гальванические элементы имеют низкую стоимость относительно аналогов, однако имеется один существенный недостаток это низкая внутренняя емкость таких батареек.
Щелочные
Состав батарейки такого вида отличается от своих аналогов применяемым электролитом, в них используется активная щелочь гидроксид калия KOH. Электрод выполнен из двуокиси таких металлов, как цинк и марганец. Нашли широкое применение в современной электронике, на корпусе элементов указывается маркировка «ALKALINE».
Основным плюсом такой батарейки является продолжительный срок службы, в процессе эксплуатации номинальное напряжение понижается с меньшей скоростью. К минусам относят повышенную стоимость.
Серебряные
В качестве электролита применяют КОН, в состав электродов включено серебро. В таких элементах отмечают значительно увеличение срока службы, повышенную энергетическую плотность, постоянное номинальное напряжение, а также полную безвредность. Недостатками являются высокая цена.
Ртутные
В строении таких батареек используется цинк в качестве металла для анода, катод выполняется из ртутного оксида. Электроды разделяются сепаратором пропитанным электролитом. Такой элемент питания способен выполнять функции аккумулятора, однако емкость будет постепенно понижаться с каждым циклом восстановления заряда. При разряде происходит слипание ртути, а при заряде образуются дендриты цинка. Во время эксплуатации не допускается разгерметизация корпуса в связи с повышенной вредностью паров ртути. К преимуществам относят сохранение длительных значений плотности энергии, емкости и напряжения.
Внимание! Ртутные источники питания являются опасными для здоровья человека и окружающей среды.
Литиевые
Данные элементы питания постепенно вытесняют все аналоги. Отрицательные электроды такой батарейки сделаны из лития. В них постоянно совершенствуются основные технические характеристики. К плюсам батареек с литиевым электродом относят увеличение срока хранения, широкий диапазон рабочих температур, повышенная внутренняя емкость. Основным минусом является повышенная стоимость.
Устройство батарейки
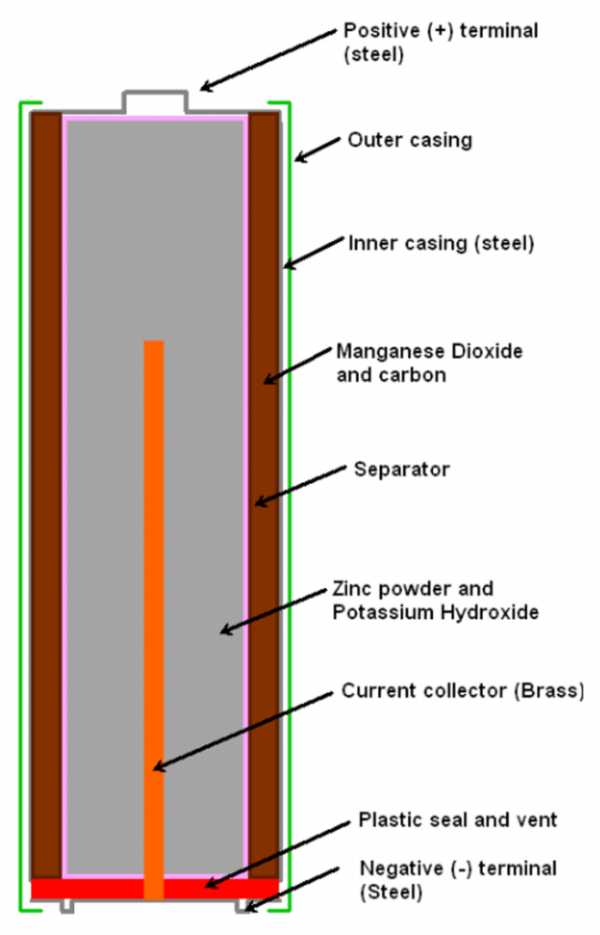
Рассмотрим, как устроена батарейка на примере щелочного элемента в разрезе. В качестве материала для отрицательного электрода применяется цинк, он пропитывается щелочным электролитом. Вывод анода на корпус изготавливается в виде стальной тарелки. Положительный электрод производят из никелированной стали.

Для того, чтобы не возникало коротких замыканий необходимо изолировать оболочку. Специальная прокладка удерживает газы, которые образуются в ходе химических реакций, так как их количество незначительно, камера для сбора выполняется малых размеров. В конструкции присутствует предохранительная мембрана, она защищает батарейку от возникновения короткого замыкания. Мембрана прорывается, и излишний электролит вытекает наружу.
Принцип работы батарейки
Любой химический источник питания имеет в своей конструкции положительно и отрицательно заряженные электроды, а также активный электролит. Заряженные частицы электроны перемещаются от минуса к плюсу при подключении нагрузки. Катод выполняет восстановительную функцию, напитываясь зарядом от анода. Жидкий или твердый электролит выполняет функцию проводника для заряженных частиц.
Интересно знать! В результате химических реакций внутри элемента питания происходит необратимое разрушение металлических элементов питания, батарейка теряет свою емкость.
Применение
Различные виды могут применяться по-разному, зависит это от их основных конструктивных свойств и характеристик:
- Элементы питания с твердым электролитом используют в устройствах с малым значением потребляемого тока. Например, часы фонарики с малой мощностью, а также пульты дистанционного управления.
- Щелочные батарейки применяют в электротехнике с повышенным значением тока, к ним можно отнести различные камеры и магнитофоны, а также игрушки с электродвигателем.
- Источники питания с серебряными электродами способны обеспечить электроэнергией в калькуляторах, переносных инструментах и аппаратах для улучшения слуха.
- Литиевые батарейки используют в портативной электронике, где необходимо стабильное значение емкости и потребляемого тока.
Выбор источника питания
Для правильного выбора элементов питания необходимо обратить внимание на следующие факторы:
- В аппаратах и оборудовании какого вида он будет применяться.
- Электролит какого состава используется в конструкции.
- Стоимость батарейки, иногда более выгодно приобрести несколько дешевых, чем один очень дорогой.
- Каждый элемент питания на корпусе имеет маркировку, по которой можно определить вид и состав источника питания.
- Необходимо ориентироваться по условиям окружающей среды в процессе эксплуатации.
- Рекомендуется приобретать источники питания, произведенные сравнительно недавно, так как с течением времени емкость может понижаться.
- Перед покупкой следует обратить внимание на целостность упаковки и самого корпуса элемента.
- Батарейка должна конструктивно соответствовать своему посадочному месту в электроприборе.
Правильный выбор и соблюдение требований к безопасной эксплуатации позволит продлить работу любого элемента питания. Для определенных видов техники необходим свой вид батарейки.
batteryzone.ru
Батарейка — устройство, принцип работы, виды
 Батарейка — это слово плотно вошло в нашу повседневную жизнь. Но, к сожалению, сегодня мало кого интересует её история, устройство, её виды. Давайте вместе разберёмся с этими и другими интересными вопросами о батарейке. А точнее «что такое батарейка», «как работает батарейка». Повседневная жизнь не требует каких-то великих усилий для включения телевизора, калькулятора, для нормальной работы настенных часов, для работы компьютерной мыши и так далее. А все благодаря каким-то батарейкам, которые помогают упростить нашу жизнь, помогают сэкономить наше время. Это понимает каждый здравомыслящий человек, но не каждый задаёт себе вопрос: «как из таких маленьких батареек совершается такой объём работы», «как устроены батарейки»… А, между тем, это физика.
Батарейка — это слово плотно вошло в нашу повседневную жизнь. Но, к сожалению, сегодня мало кого интересует её история, устройство, её виды. Давайте вместе разберёмся с этими и другими интересными вопросами о батарейке. А точнее «что такое батарейка», «как работает батарейка». Повседневная жизнь не требует каких-то великих усилий для включения телевизора, калькулятора, для нормальной работы настенных часов, для работы компьютерной мыши и так далее. А все благодаря каким-то батарейкам, которые помогают упростить нашу жизнь, помогают сэкономить наше время. Это понимает каждый здравомыслящий человек, но не каждый задаёт себе вопрос: «как из таких маленьких батареек совершается такой объём работы», «как устроены батарейки»… А, между тем, это физика.
Самые первые прототипы батареек появились ещё в Месопотамии около 2000 лет назад. Состояла она в то время из глиняной вазы, медного и железного стержней, залитыми битумом. Кстати, если такой сосуд залить кислотой (уксусной, серной), то получим напряжение примерно в 1В. Назвали такой прототип «Багдадской батарейкой » в связи с местом, на котором были обнаружены.
Примерно в 1800 году итальянский физик Алессандро Вольта изобрёл батарейку, которой мы и по сей день продолжаем пользоваться. Кстати, кто не знает что такое батарейка, так это источник питания, который вырабатывает электричество под действием химического процесса. То есть батарейка это гальванический элемент, работающий на химической реакции. Так можно объяснить и детям.
____________________________________________
Возможно, вам будет интересно: Почему батарейки кислые на вкус?
__________________________________________________________________
Как работает батарейка
 Сегодня в магазинах можно увидеть большое количество батареек, они различны по некоторым принципам, но схема работы у них одна. У любой батарейки есть положительный полюс (анод–цинк Zn), отрицательный полюс (катод–марганец Mg) и электролит (может быть сухим, жидким), именно эти элементы и являются основными элементами батарейки. Электрический ток бежит от анода (+) к катоду (—), но между ними обязательно должна быть нагрузка (лампочка, диод, двигатель или что-то ещё). Если нагрузки не будет (соединить «–» с «+» напрямую), то произойдёт короткое замыкание (К.З.).
Сегодня в магазинах можно увидеть большое количество батареек, они различны по некоторым принципам, но схема работы у них одна. У любой батарейки есть положительный полюс (анод–цинк Zn), отрицательный полюс (катод–марганец Mg) и электролит (может быть сухим, жидким), именно эти элементы и являются основными элементами батарейки. Электрический ток бежит от анода (+) к катоду (—), но между ними обязательно должна быть нагрузка (лампочка, диод, двигатель или что-то ещё). Если нагрузки не будет (соединить «–» с «+» напрямую), то произойдёт короткое замыкание (К.З.).
Катоды выполняют функцию восстановителя, т.е. принимают электроны от прибывшего анода. Электролит это среда, в которой перемещаются ионы, которые образуются в процессе химической реакции. В процессе работы батарейки постепенно образовываются новые вещества, а электроды постепенно разрушаются — батарейка садится.
Вот и вся работа батарейки, кстати, все процессы, проходящие в гальваническом элементе, необратимы, то есть заряжать батарейки нельзя. Кратко говоря о работе батарейки: анод — нагрузка — катод — электролит.
Электролит изначально изготовляли в жидком виде, но это неудобно, так как при переворачивании батарейки она просто не работала. Из-за этого электролит стали загущать, превращать его в сухой вид.
Виды батареек
- Солевые (угольно-цинковые, марганцево-цинковые) батарейки.
Изготовляются из пассивного угля и двуокиси марганца, электролит из хлорида аммония и катод из цинка. В перерывах работы элементы питания могут восстанавливаться, т.е. выравнивать локальные неоднородности в композите электролита, вызванных разрядом. Такой процесс немного продлевает срок службы батарейки.

- Алкалиновые (щёлочные) батарейки
В отличие от солевых батареек у этих химический элемент электролита — щелочной электролит. Щёлочные батарейки (алкалин) имеют продолжительный срок хранения, а в процессе эксплуатации напряжение на электродах меняется гораздо меньше, чем у элементов с солевым раствором.

- Литиевые батарейки — li ion
Самые современные. В отличие от щёлочных и солевых батареек, в состав катода входит литий (Li – наивысший отрицательный потенциал), в состав анода — различные материалы. Электролит — органический электролит. В связи с такими элементами литиевые батарейки получили большой срок хранения, большую плотность энергии и различную рабочую температуру.
что такое батарейка АА
Что такое батарейка типа АА — пальчиковые.
Что такое батарейка ААА — мизинчиковые (те, что мы привыкли использовать в пультах).
yznavai.ru
| Где-то год назад я понял, что не вполне понимаю, как работают батарейки и аккумуляторы. Попытался разобраться. Прочитал десяток-два популярных объяснений на разных образовательных сайтах, и пришел к выводу, что они часто объясняют только половину процесса, и создают ложное впечатление. Опросил друзей и знакомых и пришел к выводу, что у них, как и у меня, было это ложное впечатление. Написал следующий текст в качестве попытки его исправить и объяснить себе лучше. Поправки и уточнения от физиков, химиков, инженеров итд. принимаются с благодарностью. 1. У батарейки есть два электрода, положительный и отрицательный. На отрицательном электроде происходит химическая реакция, производящая свободные электроны. На положительном электроде происходит химическая реакция, поглощающая свободные электроны. Для разных видов батареек используют разные реакции. 2. Вместе с тем обе реакции нейтральны по отношению к заряду. Та, которая производит электроны, балансирует это тем, что также производит катионы (положительно заряженные ионы, т.е. атомы с недостающими электронами) или поглощает анионы (атомы с лишними электронами). Та, которая поглощает электроны, либо производит анионы, либо поглощает катионы. 3. Ионы (положительные катионы или отрицательные анионы), которые участвуют в этих реакциях, приходят из/уходят в электролит. Электролит — это жидкое или сухое вещество, окружающее оба электрода и заполняющее все батарейку. У разных видов батареек электролит состоит из разных соединений. Главное для электролита — следующие его свойства: 1) его молекулы очень легко расщепляются в «суп» из катионов/анионов; 2) свободные электроны не могут легко в нем передвигаться; 3) катионы/анионы, наоборот, могут в нем легко передвигаться (иногда только один из видов, иногда только в одном направлении). Реакции на электродах происходят на границе электрода и электролита. 4. Из-за разного устройства электронной оболочки разных элементов — это сильное упрощение — у каждой из двух химических реакций есть свой электрический потенциал (т.е. энергия, которая освобождается/потребляется при каждой реакции). Эти потенциалы противоположны по знаку, но они неодинаковы, и разница между ними определяет напряжение батарейки, т.е. насколько сильно она «хочет» толкать электроны. Количество самого материала для реакции не влияет на напряжение, а только на емкость батарейки. 5. Когда цепь между полюсами батарейки не замкнута, реакции на электродах не протекают (точнее, протекают очень медленно). Почему? Даже очень маленький избыток разряда создает очень мощную электростатическую силу (закон Кулона), стремящуюся его сбалансировать. Например, возьмем реакцию, которая берет отрицательные ионы из электролита и производит свободные электроны. Свободные электроны остаются на электроде, им некуда уйти (электролит не пропускает их). Даже крохотный избыток электронов на электроде и дефицит отрицательных ионов в электролите создает электростатические силы (между ними и соседними атомами в электроде/электролите), которые не дают реакции продолжаться. 6. Когда цепь замкнута, электроны текут по цепи от отрицательного электрода к положительному, и одновременно ионы текут внутри электролита, поддерживая нейтральность заряда. Внешняя цепь переносит такой-то заряд от отрицательного электрода к положительному и одновременно поток ионов внутри электролита (либо положительных в том же направлении, либо отрицательных в обратном, иногда и то и другое) переносит ровно тот же заряд в обратном направлении. Без этого потока ионов через электролит, т.е. без тока *внутри* батарейки, ничего бы не работало. 7. В дополнение к тому, что электролит сам по себе плохо пропускает электроны, внутри батарейки обычно есть «сепаратор» — пористая ткань или пластик, пропитанные электролитом. Сепаратор пропускает сквозь себя электролит, так что ионы могут проходить, но еще более затрудняет проход свободных электронов. 8. В конце концов у реакций кончается исходный материал (например, металл полностью превращается в оксид) и батарейка перестает работать. Иногда реакции так подобраны, что положительные/отрицательные ионы в них на двух электродах симметричны, и тогда электролит не разрушается со временем. В других типах батареек сам электролит тоже ухудшается со временем. 9. Если это не просто батарейка, а аккумулятор, то происходит следующее. Когда он разряжается, электроны двигаются по внешней цепи, а положительные ионы двигаются внутри электролита, и потом они соединяются заново (в другой реакции и в другое соединение) на противоположном электроде. Когда аккумулятор заряжает, внешний потенциал, который больше потенциала самого аккумулятора и действует в обратном направлении, заставляет реакции происходит в обратном направлении, и все происходит «наоборот», как будто время пустили назад: второе соединение расщепляется на электроны и позитивные ионы, позитивные ионы движутся сквозь электролит, электроны по внешней цепи, и они соединяются опять в то, что было в самом начале. P.S. Главное, что я во всем этом не понимал, и что по-моему обычно не объясняют в научно-популярных статьях и что не понимают «чайники» типа меня, это роль электролита как проводника ионов, точно балансирующих по заряду поток электронов по внешней цепи. Когда я прошу образованных людей, но не физиков-химиков-инженеров, объяснить мне на пальцах, как работает батарейка, обычно это звучит примерно так: «из-за химических реакций один полюс батарейки заряжен отрицательно, другой положительно, но между полюсами изолирующий материал и поэтому разница зарядов остается, пока не замкнут цепь, и тогда электроны будут течь из-за этой разницы зарядов». Я примерно так тоже это представлял, пока не попытался лучше понять. |
avva.livejournal.com
Батарейки. Виды и устройство. Работа и применение. Как выбрать
Батарейки являются одними из наиболее популярных и распространенных источников питания. Их часто применяют для различной электроники и мелкой техники. Это разнообразные игрушки, ручные часы, дистанционные устройства, фонари, электронные весы, бритвы, небольшие устройства с моторчиком. Потребность в этих источниках питания постоянная, поэтому в магазинах их можно встретить практически повсеместно.
Большую часть этих источников питания нельзя перезарядить, они не вечны и через некоторое время разряжаются. Но при этом один вид батареек может служить на порядок дольше, чем другие виды. Естественно, что стоят они несколько дороже. Также необходимо учитывать, что некоторые источники питания плохо держат напряжение, могут течь и даже портить электронику и другую технику. Чтобы выбрать правильные источники питания, необходимо знать их особенности и учитывать нюансы их использования.
Виды
Батарейки имеют пять основных видов. Во многом это зависит тем, какие материалы применяются при их производстве. В особенности это касается их активных компонентов, в частности электролита, катода и анода. Можно выделить следующие виды элементов питания:
- Солевые.
- Щелочные.
- Серебряные.
- Ртутные.
- Литиевые.
Особенности, плюсы и минусы
Солевые источники питания. К примеру, это Duracell и Energizer из США, «Орион» из России, Toshiba из Японии. К преимуществам таких элементов относится невысокая цена. Однако у них имеются существенные минусы — небольшая емкость заряда.
Щелочные или так называемые алкалайновые источники питания. В данном случае применяется щелочной электролит. Создателем данных элементов была фирма Duracell. Электрод здесь выполнен из двуокиси марганца и цинка, при этом в виде электролита применяется гидроксид калия. Данные источники питания особенно популярны среди создателей электроники. В большей части случаев на корпусе щелочного элемента питания пишется название «ALKALINE».
К преимуществам таких элементов относится существенный срок действия. При эксплуатации напряжение на электродах изменяется меньше. Минусом будет высокая цена, которая превосходит стоимость солевых элементов.
Серебряные. Электролитом в данном случае является гидроксид калия либо гидроксид натрия. Эксплуатационные свойства этих устройств во многом схожи с ртутными элементами. К их преимуществам относятся значительное время хранения, плотность энергии, постоянное напряжение, отсутствие токсичности, большая емкость на единицу массы. Среди минусов можно назвать достаточно высокую цену.
Ртутные. Здесь анодом выступает цинк, а катодом — оксид ртути. Их разделяют сепараторный элемент и диафрагма, которые пропитаны электролитным составом, выполненного из адсорбентированного гидроксида калия. Необходимо отметить, что ртутный элемент на цинковой основе может действовать как аккумуляторное устройство, но его емкость будет постепенно снижаться от заряда к разряду. Вызвано это слипанием ртути при разряде, а также увеличением дендритов цинка во время заряда.
К преимуществам этих элементов питания можно отнести постоянство напряжения, емкость и энергоплотность. Однако их цена достаточна высока, а ртуть токсична. Поэтому при их использовании нельзя нарушать герметичность корпуса устройства.
Литиевые источники питания. Здесь используется литиевый катод, а также органический электролит. Такие элементы выделяются значительным сроком хранения, работоспособностью при различных температурах, плотностью энергии. К минусам следует отнести сравнительно высокую цену.
Батарейки можно классифицировать по форме и размерам. В большей части случаев их разделяют по американскому стандарту, которая признана и применяется в большинстве стран мира. Вместе со стандартом США используются и другие классификации в виде международных систем ANSI, ИЭК, а также ГОСТ. Они могут различаться по диаметру и иным габаритам, химсоставу, емкостным параметрам и напряжению.
Типы
- Пальчиковые либо AA.
- Мизинчиковые либо AAA.
- Четыре А, либо AAAA.
- Дюймовочка, либо C.
- Бочка, либо D.
- Квадратная.
- Крона, либо PP3.
- Миниатюрные источники питания.
Устройство
Конструктивно щелочной элемент имеет общее строение с солевым. Однако главные части в нем располагаются в обратном порядке. Анод выполнен из цинка, который пропитан электролитом из щелочи. Сепаратор отделяет анод от общей электролитной массы. Вывод с «плюсом» сделан из стального никелированного элемента, вывод с «минусом» изготавливается в виде тарелки из стали.
Чтобы не было замыкания, оболочка изолируется. Прокладка удерживает газы, которые образуются во время работы. Камера сбора газов в данном элементе питания небольшая, так как газы здесь образуются в небольшом количестве. Предохранительная мембрана защищает от взрыва элемента питания в случае неправильной эксплуатации, к примеру, в случае короткого замыкания. Если долго и неправильно использовать элемент питания, то мембрана может порваться, вследствие чего может произойти разгерметизация. В итоге вытечет электролит.
Принцип действия
Все батарейки имеют положительный и отрицательный полюс, а также электролит. Все эти три элемента являются основой источника питания. Электроток идет от анода к катоду, однако между ними должна иметься нагрузка в виде диода или лампочки. Катод выступает в качестве восстановителя, то есть он запитывается электронами от анода. Электролит является средой, где движутся ионы, образующиеся в результате химреакции.
В процессе химреакции происходит разрушение электродов, в том числе появление новых веществ. Это приводит к тому, что емкость падает и уже невозможно использовать элемент питания по-прежнему.
Применение
Солевые батарейки применяются в часах, фонарях, где небольшое потребление электротока, в разнообразных игрушках, а также пультах дистанционного управления.
Щелочные применяются в устройствах, где требуется высокое потребление электротока, к примеру, фотоаппараты с вспышкой, видеокамеры, магнитофоны, игрушки с моторчиком, а также иные устройства.
Серебряные применяются в калькуляторах, наручных часах, различных электрических инструментах, слуховых аппаратах.
Литиевые элементы питания применяются в фотоаппаратах, мобильниках, электронных книжках, пультах дистанционного управления, устройствах, которые требуют постоянного и надежного потребления электротока.
Как выбрать батарейки
- Батарейки следует выбирать с умом. Для начала нужно определиться с видом техники, ведь разное оборудование потребляет различное количество энергии. Вследствие этого солевые элементы питания, к примеру, подойдут для дистанционного пульта управления, а для фотокамеры не подойдут. Поэтому необходимо учитывать мощность и тип источника питания
- Присмотритесь к типу электролита. Оборудованию со слабой мощностью вполне достаточно угольно-цинковых или солевых элементов питания. Для приборов средней мощности подойдут щелочные устройства. Для оборудования высокой мощности необходимо выбирать литиевые или серебряные элементы питания.
- Нельзя обходить вниманием стоимость данных устройств. Серебряные, литиевые и щелочные элементы питания выделяются высокой стоимостью, однако они могут работать длительное время. При правильной их эксплуатации они могут окупить себя несколько раз, тогда как солевые батарейки буквально за короткое время будут выходить из строя.
- Также следует присмотреться к упаковке и производителю элементов питания. В большинстве случаев изготовители всегда маркируют корпус элементов питания, чтобы покупатель мог определить тип электролита.
- При подборе элемента питания необходимо учитывать, что при различных нагрузках он будет вести себя совершенно по-разному. К тому же на функциональность будет влиять окружающая среда. Так зимой, но холоде будет ухудшаться электропроводность электролита, вследствие чего будет снижаться и его емкость.
- Необходимо учитывать тот факт, что при длительном хранении элементов питания они могут терять порядка 30% начальной емкости. Поэтому рекомендуется внимательно присмотреться к дате производства. Следует знать, что отечественные изготовители маркируют дату изготовления, а иностранные производители указывают последнюю дату использования батарейки.
- Необходимо тщательно осмотреть элементы устройства, чтобы убедиться в отсутствии дефектов, которые могут уменьшить эффективность эксплуатации.
- Подбирая источники питания для конкретного прибора, необходимо учитывать размеры посадочного пространства под них, оно может быть различным. К примеру, для пульта дистанционного управления будут нужны мизинчиковые батарейки, а для какого-нибудь плеера придется приобретать пальчиковые элементы питания. Для электронных весов, слухового аппарата или другого небольшого прибора потребуется купить таблеточные элементы питания. При этом необходимо учитывать маркировку, толщину и диаметр «таблетки», чтобы она подошла для конкретного прибора.
Похожие темы:
tehpribory.ru
Принцип работы батарейки: Как образуется ток?
Принцип работы батарейки заключается в простой химической реакции, которая происходит обычно между тремя элементами. В результате, реагирования веществ между собой, получается электрический ток. Это если говорить кратко.
Три ключевых объекта:
- Анод “+”
- Катод “-“
- Электролит
Анод или положительный полюс служит источником электронов. Обычно его изготавливают из цинка. Два электрода заставляет взаимодействовать между собой электролит. В качестве электролита выступает обычно соль, хлорид аммония или щелочь. Он может быть в сухом и жидком виде. Чтобы сделать густым это вещество производители добавляют полимерные соединения. Некоторые используют крахмал.
Принцип действия батарейки
Ток поступает с положительного полюса на отрицательный. Это происходит если к батареи подключена нагрузка. Если просто соединить плюс и минус проводом произойдет замыкание. В результате этого может быстро сесть батарейка, а также произойти возгорание.

Катод играет роль восстановителя. Он приобретает электроны от анода. В электролитной среде ионы прекрасно передвигаются и способствуют хорошей выработке тока.
Что происходит с точки зрения химии?
К примеру, в стеклянную емкость нальем раствор серной кислоты и поместим туда стержень, выполненный из цинка. На поверхности данного стержня имеются положительно заряженные ионы. А вокруг этого цинкового объекта, в растворе, скапливаются отрицательные ионы вещества. У раствора имеются силы притяжения, которые с легкостью отрывают ионы цинка. В результате жидкость получает положительный заряд, а цинковая пластина или стержень отрицательный. Из физики известно, что разность потенциалов равна напряжению. Отсюда и возникает электрический ток.
В итоге, когда происходит контакт кислотного раствора и металла на границе образуется электрическое поле. В момент его появления химическая энергия превращается в электрическую. Таков принцип работы батареи.
Через некоторое время ресурс батареи будет истощен. Все зависит от того где и как используется источник питания. Например, если от него работает фонарик, то при умеренном использовании 2-х батарей на 1,5 вольта каждая, хватит на 1 месяц. Но если вставить эти же самые батарейки в электрическую машинку, она будет работать несколько часов.
В результате всего этого можно сделать вывод что чем больше нагрузка, тем быстрее разрядиться батарейка.
Читайте так же:
Устройство батарейки
batareykaa.ru
Виды батареек и их характеристики
Виды батареек, их размеры и формы бывают совершенно разными, поэтому порой, попав в магазин, человек попросту не знает, что ему нужно. Без аккумуляторов трудно представить современную жизнь. Они находятся во всех окружающих нас бытовых приборах: часах, ноутбуках, фонариках, электрорамках для фото, детских игрушках и пультах.
Все батарейки имеют маркировку и отличаются по емкости, стоимости и внешнему виду. При покупке нужно на многое обращать внимание, чтобы не приобрести некачественный аккумулятор. Ведь такой элемент прослужит очень короткое время, а в некоторых случаях может нарушить функциональность прибора. Узнаем, какие бывают батарейки, а также разберемся в их особенностях и характеристиках.
История создания
У данных элементов питания есть своя история развития. Батарейка как гальванический элемент стала популярна в 1920-х годах. Но ее изобретателем считают Джорджеса Лекланше — именно он в 1867 году создал прообраз известного нам элемента питания. Конечно, в то время батарейка имела совершенно другой вид.

Массово выпускать их для потребителей стала компания Eveready. Сначала направленностью фирмы были владельцы радиоприемников, но вскоре новинку оценили рабочие шахт, предприятий, мореплаватели.
В 1920 году на рынке появилась всем известная компания Duracell и стала выпускать различные элементы питания, которые пользовались особенной популярностью. Они стали более компактными, легкими и главное – дешевыми. Состояли они из графитного стержня, оксида марганца и цинкового стаканчика. Принцип работы базировался на возникновении электрического импульса.
Марганцево-цинковые батарейки за счет наличия графитового стержня называли иногда угольно-цинковыми. За всю историю существования такие аккумуляторы усовершенствовались, претерпели множество изменений и новшеств. На данный момент их можно найти в любом магазине. А на смену угольным батарейкам пришли другие, о чем написано ниже.
Виды
Существует различная классификация батареек: в зависимости от типа, выдаваемого напряжения, размера, состава. Покупатель может купить все разновидности элементов питания.
Разберем классификацию, исходя из материалов, что входят в их состав (анода, катода, электролита).
Солевые
Их легко отличить по цене, ведь они являются самыми дешевыми. На рынке представлены фирмами «Дюраселл», «Сони», «Тошиба». Являются усовершенствованными марганцево-цинковыми батарейками. Желательно применять в приборах с низким потреблением напряжения: часах, весах, пультах.

Быстро разряжаются, их нельзя зарядить обратно. При длительной эксплуатации гальванический элемент может протечь. При минусовых температурах солевые аккумуляторы перестают работать. Несмотря на многие недостатки, данный продукт востребован на рынке.
Щелочные, или алкалиновые
Алкалиновые батарейки появились в 1964 году, а выпустила их фирма «Дюраселл». Электролитом выступает щелочь – гидроксид калия (КОН), отсюда и название у данного элемента питания. Щелочные аккумуляторы имеют большую мощность, нежели их солевые аналоги, они более герметичны (а значит меньше риск протекания), почти не подвержены саморазряду.

Их легко отличить от других – на упаковке присутствует надпись ALKALINE. Применяют их в детских игрушках, пультах ДУ, радио и ночниках. Недостатками считается большая масса и высокая стоимость.
Ртутные батарейки
Не получили широкого распространения из-за высокой стоимости и повышенной токсичности. Ведь они могут протечь, а ртуть опасна для человека. Но такой гальванический элемент можно перезаряжать несколько раз. Хотя со временем теряется его емкость — за счет того, что ртуть стекает и собирается каплями внутри батареи.

Достоинствами данных изделий можно назвать хорошую бесперебойную работу в суровых атмосферных условиях, длительный срок годности.
Серебряные
Работают по аналогии с ртутными аккумуляторами. Недостаток только один – очень высокая стоимость. Но при этом у них емкость на 30-50% больше, чем у литиевых батареек. Серебряные элементы питания хорошо работают при высоких и низких температурах, обладают длительным сроком службы.

Литиевые
Появились сравнительно недавно. Обладают большим сроком службы и хранения, герметичны, работают в суровых условиях, их можно перезаряжать. На данный момент это самые лучшие аккумуляторы на рынке, хотя их стоимость нельзя назвать низкой. Подходят для приборов с повышенным энергопотреблением: портативных колонок, фонарей, детских игрушек со звуковым сопровождением.

Типы батареек по размеру
Можно заметить, что размеры батареек тоже разные. По форме они бывают цилиндрическими и дисковыми. Первый вид более распространен. Существует классификация американская и европейская, которая нам привычнее.
В таблице приведем соотношение маркировки к диаметру, типу и виду батарей:
| Название по американской номенклатуре | Обиходное название | Высота изделия в мм | Ширина изделия в мм |
| А23 | Мини-мизинчиковая | 28,9 | 10,5 |
| АА | Пальчиковые. Широко применяются во многих приборах. Форма – цилиндрическая, тонкая. Возможна маркировка L – это значит, что элемент питания является щелочным | 50,5 | 14,5 |
| ААА | Мизинчиковая. Тонкая, цилиндрическая батарея, по размерам меньше пальчиковой, но используется в таких же устройствах (игрушки, фонари, часы) | 44,5 | 10,5 |
| АААА | Маленькая мизинчиковая. Очень редко встречается | 42,5 | 8,3 |
| С | Средняя. На данный момент редко используется. Цилиндрическая | 50 | 26,2 |
| D | Большая. В настоящее время мало применяется. Цилиндрическая, имеет вид бочонка | 61,5 | 34,2 |
| РР3 | Крона. Обладает самым высоким напряжением в 9V, квадратная. На данный момент почти не используется | 48,5 | 26,5 |

В зависимости от маркировки и номера на аккумуляторе можно с точностью сказать, подойдет вам этот элемент питания или нет. На большинстве указан состав электролита, то есть производитель не скрывает, солевая или щелочная это батарейка.
Размеры могут незначительно варьироваться на 1-2 мм. Это связано с тем, что изготовитель может поместить элемент питания в специальную защитную оболочку. Она защищает аккумулятор от последствий падений, негативных атмосферных явлений. На такой оболочке компании пишут основные данные, свою рекламу.
Существует еще особый вид батареек, который применяется в мелкой бытовой технике – дисковые, или таблеточные. Их тоже можно классифицировать в зависимости от модели, типа и размера. В основном они все литиевые и обладают напряжением 3V (CR2016, CR2450).
Как выбрать батарейку
В современном разнообразии видов батареек и их названий можно потеряться. Все они имеют разную стоимость, которая зависит от бренда, состава аккумулятора, его вида и мощности выдаваемого напряжения.
При покупке обратите внимание на такие детали:
- Вид элемента питания. Если вам нужна батарейка для часов, возможно, стоит обойтись дешевой солевой. Но если вы не хотите ее менять каждые полгода, то берите щелочную. В мощные приборы приобретайте литиевые элементы питания.
- Срок годности. Все батарейки склонны к саморазряду, только у солевых это сильно заметно, а у других видов — нет. В любом случае, если вы купите аккумулятор со свежим сроком изготовления, то и прослужит он дольше.
- Нужное вам напряжение. Дисковые гальванические элементы способны выдавать от 1,5 до 3 V. Этого достаточно для бесперебойной работы наручных часов или маленького карманного фонарика. Пальчиковые же способны создавать напряжение 4-6 V.
- Фирму-производителя. Иногда лучше заплатить за бренд, чем чинить устройство из-за потекшего элемента питания. К тому же, многие компании дают гарантию на свою продукцию. В таком случае не выбрасывайте чек с датой и упаковку.
На некоторых элементах питания стоит пометка «rechargable»: значит, их можно подзарядить с помощью зарядного устройства для батареек.
Многие производители техники конкретно пишут, какие марки батарей подходят для устройства. В таком случае возьмите с собой инструкцию и смело приобретайте нужный вам элемент питания.
batteryk.com

