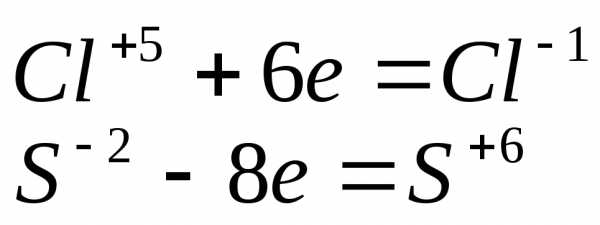Важнейшие окислители и восстановители
К
числу сильных окислителей, широко
используемых на практике, относятся
галогены (Fe2,
Cl2,
Br2,
I2),
оксид марганца Mn+4O2,
перманганат калия KMn+7O4,
манганат калия K2Mn+6O4,
оксид хрома (хромовый ангидрид) Cr+6O3,
хромат калия K2Cr+6O4,
бихромат калия K2Cr2+6O7,
азотная кислота HN+5O3 и ее соли, кислород О2,
озон О3,
перекись водорода Н2О2,
концентрированная серная кислота
Н2S+6О4,
оксид меди (II)
Сu+2О,
оксид серебра Ag2+1O,
оксид свинца Рb+4О2,
гипохлориты (например, NaCl
Щелочные и щелочноземельные металлы являются сильными восстановителями. К числу других восстановителей относятся: водород, углерод, оксид углерода С+2О, сероводород Н2S-2, оксид серы S+4О2, сернистая кислота Н2S+4О3 и ее соли, галогенводороды (кроме HF), хлорид олова (II) Sn+2Cl2, сульфат железа (II) Fe+2SO4.
Типы окислительно-восстановительных реакций. Окислительно–восстановительный эквивалент
Различают три типа окислительно–восстановительных реакций: межмолекулярные, внутримолекулярные и реакции самоокисления–самовосстановления.
Межмолекулярные – это такие реакции, в которых молекулы, атомы или ионы элементов, входящие в состав одного вещества и являющиеся окислителем, взаимодействуют с молекулами, ионами, атомами, входящих в состав другого вещества (восстановителя): например:
Во внутримолекулярных реакциях изменяется СО элементов одного и того же вещества таким образом, что одни из них окисляются, а другие — восстанавливаются. К таким реакциям относится, например, разложение бертолетовой соли и оксида ртути (II):
2KCl+5O3-2 = 2KCl-1 + 3O20;
2Hg+2O-2 = 2Hg0 + O20.
В реакциях самоокисления–самовосстановления (диспропорционирования) атомы одного и того же вещества так взаимодействуют друг с другом, что одни отдают электроны (окисляются), а другие их присоединяют (восстанавливаются). Например, растворение хлора в воде:
Cl2
(Cl0Cl0 + H2O = HCl+1O + HCl-1).
В обиход химиков, изучающих рассматриваемые процессы, наряду с химическими эквивалентами вошли окислительный и восстановительный эквиваленты. Это частное от деления молярной массы вещества на число приобретаемых (или теряемых) электронов. Так, в реакции
5H2S + 2KMnO4 + 3H3SO4 = 5S + 2MnSO4 + K2SO4 + 8H2O
для KMnO4 окислительный эквивалент равен 158,15/5, а для сероводорода восстановительный эквивалент – половине его молярной массы.
Методика составления окислительно–восстановительных реакций на основе электронного баланса
С точки зрения электронной теории окислительно–восстановительными реакциями называются такие реакции, при протекании которых происходит переход электронов от одних атомов, молекул или ионов к другим. Поскольку электроны в окислительно–восстановительных реакциях переходят только от восстановителя к окислителю, а молекулы исходных веществ и продуктов реакции электронейтральны, то число электронов, отданных восстановителем всегда равно числу электронов, принятых окислителем. Это положение называется принципом электронного баланса и лежит в основе нахождения коэффициентов в уравнениях окислительно–восстановительных реакций.
Согласно этому принципу число молекул окислителя и число молекул восстановителя в уравнении окислительно-восстановительных реакций должны быть такими, чтобы количество принимаемых и отдаваемых электронов было одинаковым.
Рассмотрим применение принципа электронного баланса при нахождении коэффициентов в уравнениях окислительно–восстановительных реакций на конкретных примерах.
При каталитическом окислении аммиака NH3 кислородом О2 образуется оксид азота NO и вода Н
NH3 + O2 NO + H2O.
Над символами элементов, изменяющих в процессе реакции СО, подпишем их значения:
N-3H3 + O20 N+2O-2 + H2O-2.
Из изменения величины СО видно, что азот в молекуле аммиака окислился, а молекула кислорода – восстановилась, то есть аммиак является восстановителем, а кислород – окислителем. Из этой схемы также вытекает, что атом азота, изменяя СО от -3 до +2, отдает кислороду пять электронов. Поскольку водород СО не меняет, то молекула аммиака будет отдавать всего 5 электронов. Атом кислорода принимает 2 электрона (СО меняется от 0 до -2), следовательно, молекула кислорода будет принимать 4 электрона. Запишем указанные процессы в виде схемы:
N-3 — 5ē N+2 5
20
O20 + 4ē 2O-2 4
4 окисление – восстановитель
5 восстановление — окислитель
Согласно принципу электронного баланса количества молекул окислителя и восстановителя нужно взять такими, чтобы числа принимаемых и отдаваемых электронов были равными. Для этого находится общее кратное, а затем делится на число отдаваемых или приобретаемых электронов; полученные коэффициенты ставятся соответственно перед молекулой восстановителя и окислителя. Из этой схемы видно, что 4 молекулы NH3 отдают 20 электронов, которые принимаются 5 молекулами О2. Коэффициенты электронного баланса называются основными коэффициентами. Они никаким изменениям не подлежат:
4NH3 + 5O2 NO + H2O.
Все остальное уравнивается в соответствии с их величиной:
4NH3 + 5O2 4NO + 6H2O.
При окислении сульфида мышьяка As2S3 азотной кислотой HNO3 образуются мышьяковистая кислота H3AsO4, серная H2SO4 и оксид азота NO.
Составим схему реакции, указывая СО над символами тех элементов, у которых в процессе реакции они изменяются:
As2+3S3-2+ HN+5O3 H3As+5O4 + H2S+6O4 + N+2O.
Подсчитаем количество электронов, отдаваемых молекулой восстановителя и принимаемых молекулой окислителя. Мышьяк изменяет СО от +3 до +5, отдавая 2 электрона. Два атома в молекуле мышьяка As 2S3 отдадут 4 электрона. Сера меняет СО от -2 до +6, отдавая 8 электронов. Три атома серы этой молекулы отдают 24 электрона. Всего одна молекула As2S3 отдает 28 электронов. Принимает электроны азот в HNO3, изменяя СО от +5 до +2. Следовательно, каждая молекула HNO3 принимает 3 электрона. Запишем это в виде схемы:
As2+3S3-2 — 28ē = 2As+5 + 3S+6 (окисление) 84 N+5 + 3ē = N2+ (восстановление) | 3 |
Очевидно, что для соблюдения электронного баланса надо взять 3 молекулы As2S3 (3·28=84) и 28 молекул HNO3 (3·28=84), все остальные коэффициенты уравниваются в соответствии с этими основными коэффициентами:
3As2S3 + 28HNO3 => 6H3AsO4 + 9H2SO4 + 28NO.
Подсчет атомов водорода показывает, что в левой части их 28, а в правой – 36. Кислорода в правой части 84 атома, в правой – 88. Если водород или кислород не входят в уравнение реакции в виде простых веществ, то они уравниваются добавлением нужного количества молекул воды в ту часть уравнения, где их недостает. Поэтому подсчет атомов кислорода или водорода проводят в последнюю очередь, причем уравнивание водорода добавлением молекул воды приводит к автоматическому уравниванию кислорода и наоборот. Если водород или кислород входят в уравнение реакции в виде простых веществ, то их необходимо уравнивать независимо друг от друга.
Окончательно рассматриваемое уравнение реакции будет иметь вид:
3As2S3 + 28HNO3+ 4Н2О = 6H3AsO4+ 9H2SO4 + 28NO.
Если числа электронов, отдаваемых молекулой восстановителя и принимаемых молекулой окислителя, имеют общий делитель, то на него можно сократить основные коэффициенты, например:
| 8 24 6 | 4 | (восстановление) (окисление) |
Наибольший общий делитель равен 2. Коэффициенты в уравнении будут
4HСlO3 + 3H2S = 4HCl + 3H2SO4.
Электронный баланс в данном случае .
4. Если число участвующих в реакции атомов нечетное, а в результате ее должно получиться четное число атомов хотя бы одного из изменяющихся СО элементов, то основные коэффициенты удваиваются:
3 3 1 | 6 2 | (окисление) (восстановление) |
6FeSO4 + 2HNO3 + 3H2SO4 = 3Fe2(SO4)3 + 2NO + 4H2O.
В рассмотренном примере в протекании окислительно-восстановительной реакции принимает участие серная кислота. Она необходима для связывания образовавшегося трехвалентного железа. Нужное количество молекул H2SO4 определяется после расстановки коэффициентов перед продуктами реакции в соответствии с основными коэффициентами в левой части уравнения. Водород или кислород уравниваются в последнюю очередь добавлением молекул воды.
5. Окислитель или восстановитель, кроме основной окислительно-восстановительной реакции, расходуется также на связывание образующихся продуктов реакции. Например:
1
3 группы по два иона хлора, всего шесть ионов хлора
(восстановление)
(окисление)
K2Cr2O7 + 6HCl 2CrCl3 + 3Cl2 + 2KCl.
На связывание продуктов реакции в соответствии с основными коэффициентами необходимо 8 молекул HCl, которые не окисляются (на образование 2 молекул CrCl3 и 2 молекул KCl). Таким образом:
K2Cr2O7 + 6HCl + 8HCl 2CrCl3 + 3Cl2 + 2KCl.
на восстановление на связывание
Уравниваем водород или кислород, добавив в правую часть уравнения 7 молекул воды H2O, и получим окончательно:
K2Cr2O7 + 14HCl 2CrCl3 + 3Cl2 + 2KCl + 7H2O.
6.
8
2
4
1
(окисление)
(восстановление)
Основные коэффициенты 4 и 1:
4Сa + HNO3 4Ca(NО3)2 + NH4NO3.
На связывание продуктов реакции требуется в соответствии с основными коэффициентами 9 молекул HNO3:
4Сa + HNO3 + 9HNO3 4Ca(NО3)2 + NH4NO3 + 3H2O.
на окисление на связывание
7. Оба элемента — и отдающий и принимающий электроны — находятся в одной молекуле. Для нахождения основных коэффициентов подобные процессы рассматривают как бы идущими справа налево:
6 24 4 | 4 6 | 2 3 | (окисление) (восстановление) |
2KСlO3 = 2KCl + 3O2.
8. Один и тот же элемент окисляется и восстанавливается. Такие реакции называются реакциями диспропорционирования. В этом случае, так же как и в предыдущем, электронный баланс составляется справа налево:
4K2SO3+4 = 3K2SO4+6 + K2S-2
S+6 + 2ē = S+4 12 S-2— 6ē = S+4 | 6 2 | 3 (восстановление) 1 (окисление) |
Рассмотренный способ подбора коэффициентов в окислительно–восстановительных реакциях не является единственным. Существуют и другие способы. Однако во всех случаях главным остается нахождение основных коэффициентов электронного баланса.
Литература:
Глинка Н.Л. Общая химия. – М.: Химия, 1978. — С. 261-270.
Карапетьянц М.Х. Введение в теорию химических процессов. – М.: Высшая школа, 1981. — С. 90-106.
Шиманович И.В., Павлович М.Л., Тикавый П.Ф., Малашко П.М. Общая химия в формулах, определениях, схемах. – Мн.: Унiверсiтэцкае, 1996. — С. 14-32.
Кудрявцев А.А. Составление химических уравнений. – М.: Высшая школа, 1991. – 264 С.
Воробьев В.К., Елисеев С.Ю., Врублевский А.В. Практические и самостоятельные работы по химии. – Мн.: УП «Донарит», 2005. — С. 4-9, 65-75.
studfile.net
Окислители и восстановители
По их функции в окислительно-восстановительных процессах их участники делятся на окислителей и восстановителей.
Окислители– это атомы, молекулы или ионы, принимающие электроны от других атомов. Степень окисления окислителя уменьшается.
Восстановители– атомы, молекулы или ионы, отдающие электроны другим атомам. Степень окисления восстановителя повышается. При протекании ОВР окислитель восстанавливается, восстановитель – окисляется, причем оба процесса протекают одновременно.
Соответственно, окислители и восстановители взаимодействуют в таких соотношениях, чтобы числа принятых и отданных электронов были одинаковы.
Конкретное проявление окислительных или восстановительных свойств атомами различных элементов зависит от многих факторов. К важнейшим из них следует отнести положение элемента в таблице Менделеева, степень окисления элемента в данном веществе, особые свойства других участников реакции (характер среды для растворов, концентрация реагентов, температура, стереохимические свойства сложных частиц и др.)
Окислители.
Окислителями могут быть как простые, так и сложные вещества. Попытаемся определить, какие факторы определяют окислительные (и восстановительные) свойства веществ.
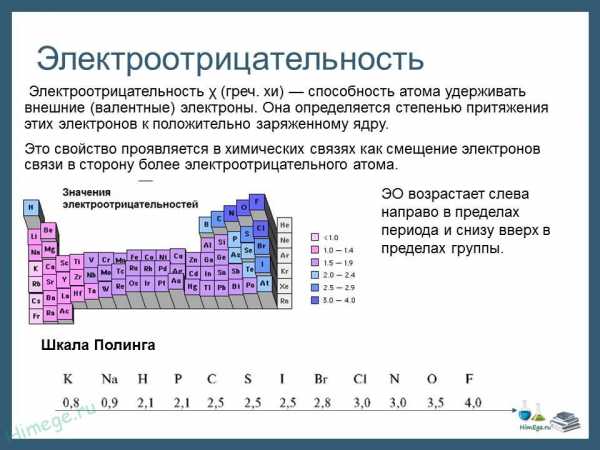
Об окислительной способности простых веществ можно судить по значениям относительной электроотрицательности (χ). Это понятие отражает способность атома смещать к себе электронную плотность от других атомов, т.е. фактически является мерой окислительной способности простых веществ. Действительно, наиболее сильные окислительные свойства проявляют активные неметаллы с максимальными значениями электроотрицательности. Так,фтор F2 проявляет только свойства окислителя, поскольку имеет самое большое значениеχ, равное 4,1 (по шкале Оллреда-Рохова). Второе место занимает кислород О2, для негоχ = 3,5, еще более сильные окислительные свойства проявляет озон О3. Третье место занимает азот (χ =3,07), но его окислительные свойства проявляются только при высоких температурах, поскольку молекула азотаN2обладает очень высокой прочностью, т.к. атомы связаны тройной связью. Достаточно сильные окислительные свойства имеют хлор и бром.
С другой стороны, минимальные значения электроотрицательности присущи металлам (χ= 0,8—1,6). Это означает, что собственные электроны атомов металлов удерживаются очень слабо и легко могут переходить к атомам с большей электроотрицательностью. Атомы металлов в нулевой степени могут проявлятьтолько восстановительныесвойства и не могут принимать электроны. Наиболее выраженные восстановительные свойства проявляют металлыIА иIIА групп.
Окислительно-восстановительные свойства сложныхвеществ
Критерием окислительной способности атомов может служить степень окисления. Максимальная степень окисления соответствует переходу всех валентных электронов к другим атомам. Такой атом больше не может отдавать электроны, а может только принимать их. Таким образом, в максимальной степени окисления элемент может проявлять только окислительные свойства. Тем не менее, необходимо отметить, что максимальная степень окисления не означает автоматическое проявление ярко выраженных окислительных свойств. Чтобы реализовались свойства сильного окислителя, частица должна быть неустойчивой, максимально несимметричной, с неравномерным распределением электронной плотности. Так, в разбавленных растворах сульфат-ионSO42-, содержащий атом серы в максимальной степени окисления+6 , вообще не проявляет окислительных свойств, так как имеет высокосимметричное тетраэдрическое строение. Тогда как в концентрированных растворах серной кислоты заметная доля частиц находится в виде недиссоциированных молекул и ионовHSO4—, имеющих несимметричное строение с неравномерным распределением электронной плотности. Как следствие этого, концентрированная серная кислота, особенно при нагревании, очень сильный окислитель.
С другой стороны, минимальная степень окисления элемента означает, что атом неметалла принял максимально возможное число электронов на валентные подуровни и больше не может принимать электроны. Следовательно,
атомы неметаллов в минимальной степени окисления могут проявлять только восстановительные свойства.
Можно напомнить, что минимальная степень окисления неметалла равна номеру группы –8. Как и в случае с серной кислотой, для реализации восстановительных свойств недостаточно иметь только минимальную степень окисления. В качестве примера можно привести азот в степени окисления –3. Высокосимметричный ион аммонияNH4+в растворе крайне слабый восстановитель. Молекула аммиака, обладающая меньшей симметричностью, проявляет достаточно сильные восстановительные свойства при нагревании. Можно привести реакцию восстановления из оксидов:
3FeO+ 2NH3= 3Fe+3H2O+N2.
Что же касается простых веществ с промежуточными значениями электроотрицательности (χ =1,9 – 2,6), то для неметаллов можно ожидать реализации и окислительных, и восстановительных свойств. К таким веществам относятся водородH2, углеродC, фосфорP, сераS, иодI2и другие неметаллы средней активности. Естественно,металлыиз этой категории простых веществ исключаются, так какне могут принимать электроны.
Эти вещества при взаимодействии с активными окислителями проявляют свойства восстановителей, а при реакциях с восстановителями проявляют свойства окислителей. В качестве примера приведем реакции серы:
0 0 +4 -2 0 0 +2 -2
S+O2=SO2Fe+S=FeS
как видно, в первой реакции сера—восстановитель, а во второй—окислитель.
Сложные вещества, содержащие атомы в промежуточных степенях окисления, также будут проявлять свойства и окислителей и восстановителей. Таких веществ очень много, поэтому назовем лишь наиболее часто встречающиеся. Это соединения серы (+4): в кислой среде SO2, а в щелочной и нейтральнойSO32- иHSO3—. Если эти соединения участвуют в реакции в качестве восстановителей, то они будут окисляться до серы +6 ( в газовой фазе доSO3, а в растворе доSO42-. Если же соединения серы (+4) реагируют с активными восстановителями, то происходит восстановление до элементарной серы, или даже до сероводорода.
SO2+ 4HI=S+ 2I2+2H2O
Многие соединения азота также проявляют окислительно-восстановительную двойственность. Представляет определенный интерес поведение нитрит-ионов NO2—. При их окислении образуется нитрат-ионNO3—, а при восстановлении газообразный монооксид азотаNO. Пример: 2NaNO2+ 2NaI+2H2SO4=I2+NO+ 2Na2SO4+2H2O.
Рассмотрим еще один пример, на этот раз возьмем пероксид водорода, в котором степень окисления кислорода (-1). Если имеет место окисление этого вещества, то степень кислорода повысится до 0, и будет наблюдаться выделение газообразного водорода:
H2O2+Cl2= 2HCl+O2.
В реакциях окисления степень окисления кислорода в пероксидах понижается до (-2), что соответствует или воде H2O, или гидроксид –ионуOH— . В качестве примера приведем реакцию, часто используемую в реставрационных работах, при которых черный сульфид свинца при действии разбавленного раствора пероксида водорода превращается в белый сульфат:PbS(черный)+4H2O2=PbSO4(белый)+4H2O.
Таким образом, завершая вводную часть, приведем основные окислители, восстановители и вещества, могущие проявлять и окислительные и восстановительные свойства.
Окислители:F2,O2,O3,Cl2,Br2,HNO3,H2SO4(конц. ),KMnO4,K2Cr2O7,PbO2,NаBiO3, ионы в водном раствореFe3+,Cu2+,Ag+.
Восстановители:H2S,(S2-),HI(I—),HBr(Br—),HCl(слабый ),NH3(при высоких температурах), ионы в водном раствореFe2+,Cr2+,Sn2+и др.
Вещества с двойственными свойствами:H2 ,C,P,As,S,I2,CO,H2O2,Na2O2,NaNO2,SO2(SO32-) и, формально, практически все вещества, содержащие атомы с промежуточной степенью окисления.
Составление уравнений окислительно-восстановительных реакций.
Существует несколько способов составления уравнений ОВР. Обычно применяются
а) метод электронного баланса,
б) метод электронно-ионного баланса.
В основе обоих методов лежит нахождение таких количественных отношений между окислителем и восстановителем, при которых соблюдается равенство принятых и отданных электронов.
Метод электронного баланса является более универсальным, хотя и менее наглядным. Он основан на подсчете изменения степеней окисления атомов окислителя и восстановителя в исходных и конечных веществах. При работе с этим методом удобно следовать такому алгоритму.
Записывается молекулярная схема окислительно-восстановительной реакции,
Рассчитываются степени окисления атомов (обычно тех, которые ее меняют),
Определяются окислитель и восстановитель,
Устанавливаются числа электронов, принимаемых окислителем, и число электронов, отдаваемых восстановителем,
Находятся коэффициенты, при домножении на которые числа отданных и принятых электронов уравниваются,
Подбираются коэффициенты для других участников реакции.
Рассмотрим реакцию окисления сероводорода.
-2 0 +4 -2 -2
H2S+O2=SO2+H2O
В этой реакции сера (-2) является восстановителем, а молекулярный кислород — окислителем. Затем составляем электронный баланс.
S-2-6e—→S+4 2 — коэффициент домножения для восстановителя
O2+4e—→2O-2 3 — коэффициент домножения для окислителя
Записываем формулы веществ с учетом коэффициентов домножения
2H2S+ 3O2= 2SO2+2H2O
Рассмотрим еще один случай – разложение нитрата алюминия Al(NO3)3. В этом веществе атомы азота имеют высшую степень окисления (+5), а атомы кислорода – низшую (-2). Отсюда следует, что азот будет окислителем, а кислород – восстановителем. Составляем электронный баланс, зная, что весь азот восстанавливается до диоксида азота, а кислород окисляется до молекулярного кислорода. С учетом чисел атомов запишем:
3N+5+3e—→ 3N+44
2O-2-4e—→O2o3
тогда уравнение разложения запишется так: 4Al(NO3)3=Al2O3+ 12NO2+ 3O2.
Метод электронного балансаобычно используют для определения коэффициентов в ОВР, протекающих в гетерогенных системах, содержащих твердые вещества или газы.
Для реакций, протекающих в растворах, обычно применяется метод электронно-ионного баланса, который учитывает влияние различных факторов на состав конечных продуктов.
Данный метод учитывает: а) кислотность среды, б)концентрации реагирующих веществ, в) реальное состояние реагирующих частиц в растворе, г) влияние температуры и др. Кроме того, для данного метода нет необходимости использовать степень окисления.
studfile.net
Конспект «Окислители и восстановители» — УчительPRO
Окислители и восстановители
Ключевые слова конспекта: окислители, восстановители, окисление, восстановление.
Окислитель – вещество, атомы, молекулы или ионы которого принимают электроны. Восстановитель – вещество, атомы, молекулы или ионы которого отдают электроны. Окислителем и восстановителем могут также называть элементы, атомы которых отдают или принимают электроны. Если элемент является окислителем – его степень окисления понижается; если элемент является восстановителем – его степень окисления повышается.
Окисление – процесс отдачи электронов атомом, молекулой или ионом, степень окисления элемента повышается. Восстановление – процесс приёма электронов атомом, молекулой или ионом, степень окисления элемента понижается.
Окислители
Среди простых веществ окислительные свойства характерны для типичных неметаллов (F2, Cl2, Вг2, I2, O2, О3). Галогены, выступая в качестве окислителей, приобретают степень окисления –1, причём от фтора к йоду окислительные свойства ослабевают. Кислород, восстанавливаясь, приобретает степень окисления –2 (Н2O или ОН–).
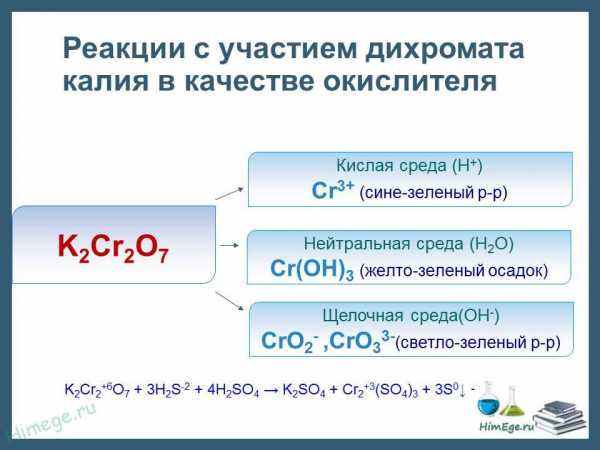
Среди кислородсодержащих кислот и их солей к наиболее важным окислителям относятся концентрированная серная кислота, азотная кислота и нитраты, перманганаты МnO4–, хроматы СrO42– и дихроматы Сr2O72–.
Концентрированная серная кислота проявляет окислительные свойства за счёт серы в высшей степени окисления +6. Продуктами восстановления серы могут быть: SO2 (степень окисления серы +4), сера – простое вещество (степень окисления серы 0), сероводород (степень окисления серы –2).
Азотная кислота проявляет окислительные свойства за счёт азота в высшей степени окисления +5, причём окислительная способность HNO3 усиливается с ростом её концентрации. Состав продуктов восстановления азотной кислоты зависит от активности восстановителя, концентрации кислоты и температуры системы; чем активнее восстановитель и ниже концентрация кислоты, тем глубже происходит восстановление азота.
Кислородсодержащие кислоты галогенов (например, HClO, HClO3, НВrO3) и их соли, действуя в качестве окислителей, обычно восстанавливаются до степени окисления галогена –1 (в случае хлора и брома) и 0 (в случае иода). Например:
5КСlO3 + 6Р = 5КCl + 3Р2O5
Водород в степени окисления +1 выступает как окислитель преимущественно в растворах кислот (как правило, при взаимодействии с металлами, расположенными в раду напряжений до водорода):
Zn + H2SO4 (разб.) = ZnSO4 + Н2↑
При взаимодействии с сильными восстановителями в качестве окислителя может проявлять себя и водород, входящий в состав воды:
2Н2O + 2Na = 2NaOH + Н2↑
Н2O + NaH = NaOH + Н2↑
Ионы металлов, находящихся в высшей степени окисления (например, Fe3+, Hg2+, Cu2+), выполняя функцию окислителей, превращаются в ионы с более низкой степенью окисления:
2FeCl3 + H2S = 2FeCl2 + S + 2HCl
Восстановители
Среди простых веществ к типичным восстановителям принадлежат активные металлы (щелочные и щёлочноземельные, алюминий, цинк, железо и др.), а также некоторые неметаллы, такие, как водород, углерод (в виде угля или кокса), фосфор, кремний. При этом в кислой среде металлы окисляются до положительно заряженных ионов.
Углерод чаще всего окисляется до монооксида СО или диоксида СO2; фосфор при действии сильных окислителей окисляется до ортофосфорной кислоты Н3РO4.
В бескислородных кислотах (НCl, НВг, HI, H2S) и их солях восстановителями являются анионы, которые, окисляясь, обычно образуют простые вещества. В ряду галогенид-ионов восстановительные свойства усиливаются от Cl– к I–.
Металлы в промежуточной степени окисления (ионы Sn2+, Fe2+, Cu+, Hg2+ и др.), взаимодействуя с окислителями, способны повышать свою степень окисления:
2FeCl2 + Cl2 = 2FeCl3
10FeSO4 +2KMnO4 + 8H2SO4 = 2MnSO4 + 5Fe2(SO4)3 + K2SO4 + 8H2O.
Образец выполнения задания ОГЭ.
Задание. Степень окисления азота в аммиаке и нитрате калия соответственно
1) –2 и +5
2) –3 и +5
3) +3 и +5
4) –4 и +3
Решение. Определим степени окисления элементов в аммиаке и нитрате натрия:
Обратим внимание, что в аммиаке степень окисления азота – отрицательная, так как электроотрицательность азота выше, чем электроотрицательность водорода.
Правильный ответ: 2) –3 и +5.
Конспект урока по химии «Окислители и восстановители».
Темы, связанные с настоящим конспектом:
uchitel.pro
| | Адрес этой страницы (вложенность) в справочнике dpva.ru: главная страница / / Техническая информация / / Химический справочник / / Горение и взрывы. Окисление и восстановление. / / Важнейшие восстановители и окислители (коротко и подробно) Поделиться:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
dpva.ru
| 1. |
Выбери процесс
Сложность: лёгкое |
1 |
| 2. |
Окисление или восстановление
Сложность: лёгкое |
1 |
| 3. |
Окисление и восстановление
Сложность: лёгкое |
1 |
| 4. |
Окислитель или восстановитель
Сложность: среднее |
2 |
| 5. |
Окислитель и восстановитель
Сложность: среднее |
2 |
| 6. |
Допиши схему окислительно-восстановительного процесса
Сложность: среднее |
2 |
| 7. |
Является ли реакция окислительно-восстановительной?
Сложность: сложное |
3 |
| 8. |
Определи окислитель
Сложность: сложное |
4 |
| 9. |
Определи степень окисления
Сложность: сложное |
4 |
www.yaklass.ru
Электроотрицательность. Степень окисления и валентность химических элементов. Реакции окислительно — восстановительные.
Окислительно-восстановительные реакции
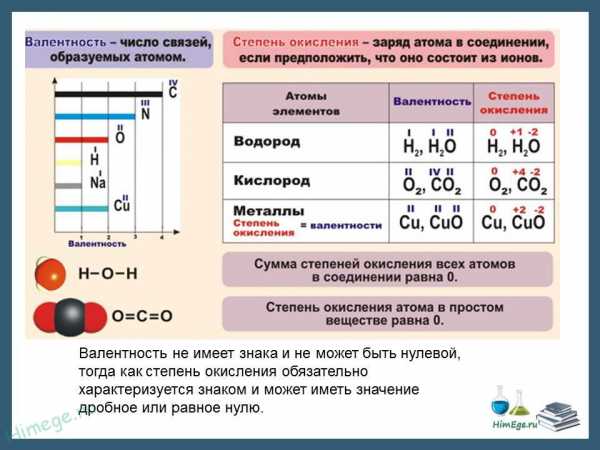
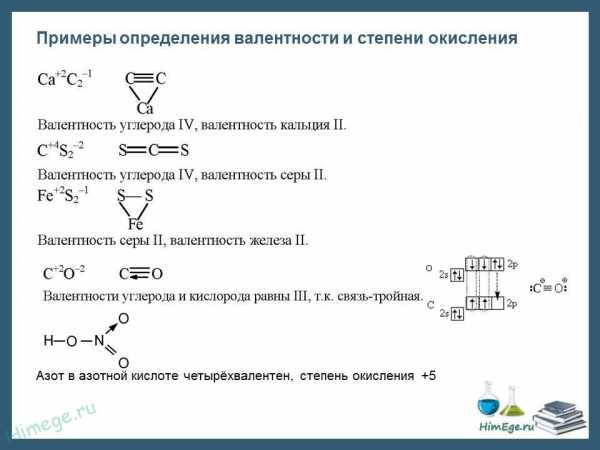
Одним из основных понятий неорганической химии является понятие о степени окисления (СО).
Степенью окисления элемента в соединении называется формальный заряд атома элемента, вычисленный из предположения, что валентные электроны переходят к атомам с большей относительной электроотрицательностью (ОЭО) и все связи в молекуле соединения являются ионными.
Степень окисления элемента Э указывают вверху над символом элемента со знаком « + » или « -» перед цифрой.
Степень окисления ионов, реально существующих в растворе или кристаллах, совпадает с их зарядовым числом и обозначается аналогично со знаком « + » или « » после цифры, например, Са2+.
Применяют также метод Штока обозначения степени окисления римскими цифрами после символа элемента: Mn (VII), Fe (III).
Вопрос о знаке степени окисления атомов в молекуле решается на основании сопоставления электроотрицательностей связанных между собой атомов, которые образуют молекулу. При этом атом с меньшей электроотрицательностью имеет положительную степень окисления, а с большей электроотрицательностью отрицательную.
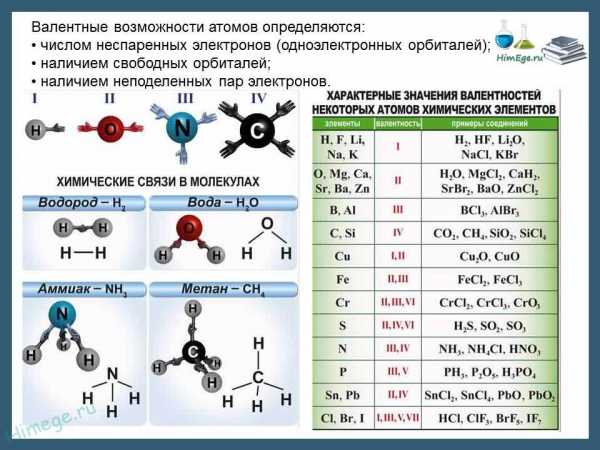
Следует отметить, что нельзя отождествлять степень окисления с валентностью элемента. Валентность, определяемая как число химических связей, которыми данный атом соединен с другими атомами, не может равняться нулю и не имеет знака « + » или « ». Степень окисления может иметь как положительное, так и отрицательное значение, а также принимать нулевое и даже дробное значение. Так, в молекуле СO2 степень окисления С равна +4, а в молекуле СН4 степень окисления С равна 4. Валентность же углерода и в том, и в другом соединении равна IV.
Несмотря на указанные выше недостатки, использование понятия степени окисления удобно при классификации химических соединений и составлении уравнений окислительно-восстановительных реакций.
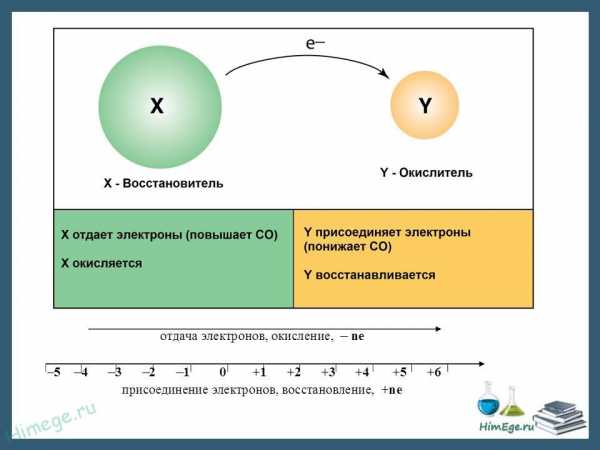
При окислительно-восстановительных реакциях протекают два взаимосвязанных процесса: окисление и восстановление.
Окислением называется процесс потери электронов. Восстановлением процесс присоединения электронов.
Вещества, атомы или ионы которых отдают электроны, называются восстановителями. Вещества, атомы или ионы которых присоединяют электроны (или оттягивают к себе общую пару электронов), называются окислителями.
При окислении элемента степень окисления увеличивается, иначе говоря, восстановитель при реакции повышает степень окисления.
Наоборот, при восстановлении элемента степень окисления понижается, т. е. при реакции окислитель уменьшает степень окисления.
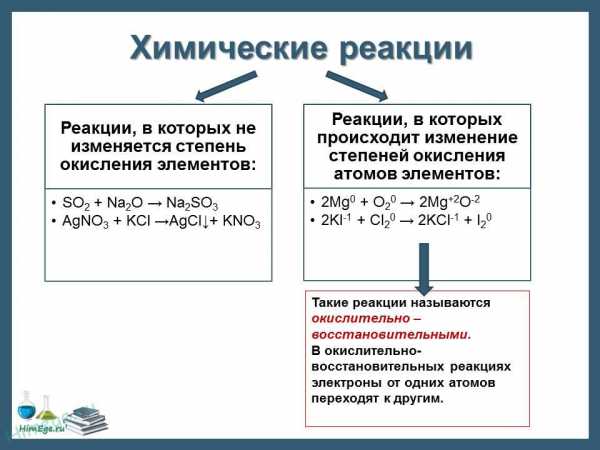
Таким образом, можно дать и такую формулировку окислительно-восстановительных реакций: окислительно-восстановительными реакциями называются реакции, протекающие с изменением степени окисления атомов элементов, входящих в состав реагирующих веществ.
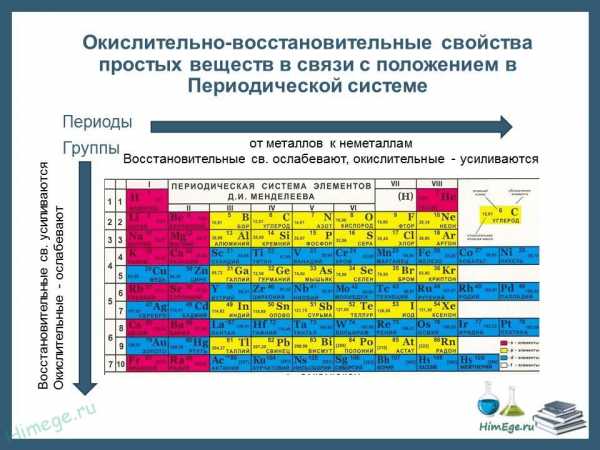
Окислители и восстановители
Для прогноза продуктов и направления окислительно-восстановительных реакций полезно помнить, что типичными окислителями являются простые вещества, атомы которых имеют большую ОЭО > 3,0 (элементы VIA и VIIAгрупп). Из них наиболее сильные окислители фтор (ОЭО = 4,0), кислород (ОЭО = 3,0), хлор (ОЭО = 3,5). К важным окислителям относятся PbO2 , KMnO4 , Cа(SO4)2 , К2Сr2O7 , HClO, HClO3, КСIO4, NaBiO3, H2SO4(конц), HNO3(конц) , Na2O2 , (NH4)2S2O8 , КСIO3 , H2O2 и другие вещества, которые содержат атомы с высшей или высокой СО.
К типичным восстановителям относятся простые вещества, атомы которых имеют малую ОЭО < 1,5 (металлы IA и IIAгрупп и некоторые другие металлы). К важным восстановителям относятся H2S, NH3, HI, KI, SnCl2 , FeSO4 , C, H2 , CO, H2SO3 , Cr2(SO4)3 , CuCl, Na2S2O3 и другие вещества, которые содержат атомы с низкими СО.
Вещества, содержащие атомы в максимальной и минимальной степенях окисления, могут быть соответственно только окислителями, например К2Сг2O7 , КМпO4 , PbO2 , HClO4 или только восстановителями, например NH3 , H2S, HI.
Вещества, содержащие атомы в промежуточных степенях окисления, способны как повышать, так и понижать степень окисления, т. е. могут быть как восстановителями (при действии более активного, чем они, окислителя), так и окислителями (при действии более активного, чем они, восстановителя). Такие вещества проявляют окислительно-восстановительную двойственность.
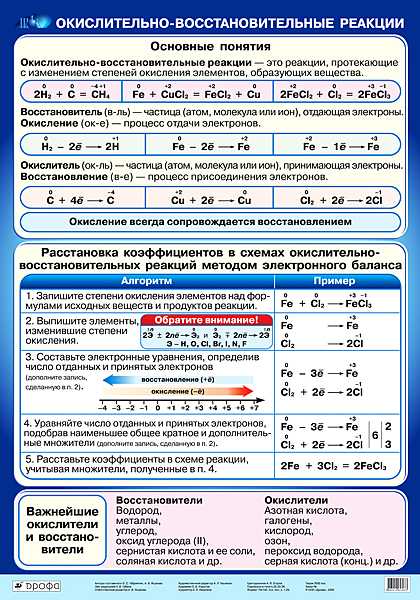
При составлении уравнений окислительно-восстановительных реакций можно применять два метода: метод электронного баланса и ионно-электронный метод (метод полуреакций). Более правильное представление об окислительно-восстановительных процессах в растворах дает ионно-электронный метод. С помощью этого метода прогнозируют изменения, которые претерпевают реально существующие в растворе ионы и молекулы.
Помимо прогнозирования продуктов реакции, ионные уравнения полуреакций необходимы для понимания окислительно-восстановительных процессов, протекающих при электролизе и в гальванических элементах. Этот метод отражает роль среды как участника процесса. И наконец, при использовании этого метода необязательно заранее знать все образующиеся вещества, так как многие из них получаются при составлении уравнения окислительно-восстановительных реакций.
Следует иметь в виду, что хотя полуреакции отражают реальные процессы, идущие при окислительно-восстановительных реакциях, их нельзя отождествлять с реальными стадиями (механизмом) окислительно-восстановительных реакций.
На характер и направление окислительно-восстановительных реакций влияют многие факторы: природа реагирующих веществ, реакция среды, концентрация, температура, катализаторы.










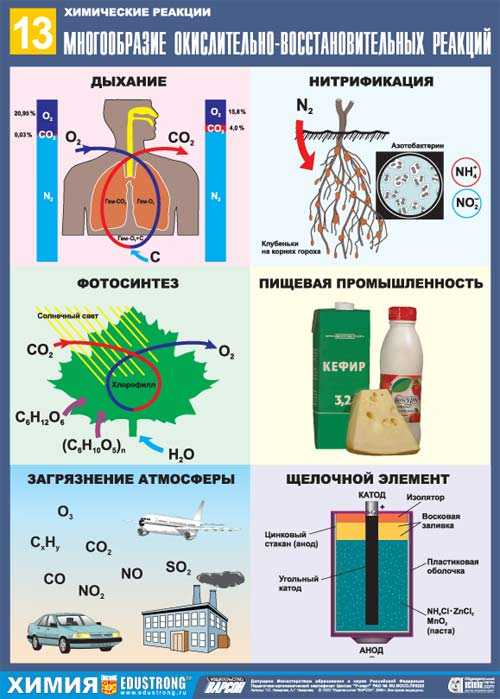
Биологическое значение окислительно-восстановительных процессов
Важными процессами в животных организмах являются реакции ферментативного окисления веществ-субстратов: углеводов, жиров, аминокислот. В результате этих процессов организмы получают большое количество энергии. Приблизительно 90% всей потребности взрослого мужчины в энергии покрывается за счет энергии, вырабатываемой в тканях при окислении углеводов и жиров. Остальную часть энергии ~10% дает окислительное расщепление аминокислот.
Биологическое окисление протекает по сложным механизмам при участии большого числа ферментов. В митохондриях окисление происходит в результате переноса электронов от органических субстратов. В качестве переносчиков электронов в дыхательную цепь митохондрий входят различные белки, содержащие разнообразные функциональные группы, которые предназначены для переноса электронов. По мере продвижения по цепи от одного интермедиата к другому электроны теряют свободную энергию. На каждую пару электронов, переданных по дыхательной цепи кислороду, синтезируются 3 молекулы АТФ. Свободная энергия, высвобождающаяся при переносе 2 электронов на кислород, составляет 220 кДж/моль.
На синтез 1 молекулы АТФ в стандартных условиях расходуется 30,5 кДж. Отсюда ясно, что довольно значительная часть свободной энергии, выделяющейся при переносе одной пары электронов, запасается в молекулах АТФ. Из этих данных становится понятной и роль многостадийной передачи электронов от исходного восстановителя к кислороду. Большая энергия (220 кДж), выделяемая при переносе одной пары электронов к кислороду, разбивается на ряд порций, соответствующих отдельным стадиям окисления. На трех таких стадиях количество выделяющейся энергии примерно соответствует энергии, необходимой для синтеза 1 молекулы АТФ.
himege.ru
Окислители и восстановители
Окислителями называют соединения или простые вещества,  которые в процессе химической реакции присоединяют к себе электроны.
которые в процессе химической реакции присоединяют к себе электроны.
Восстановителями называют соединения или простые вещества, отдающие свои электроны.
Окислительные и восстановительные реакции идут параллельно, так что количество отсоединенных и присоединенных электронов одинаково. При этом окислитель восстанавливается, а восстановитель — окисляется.
Окислителем или восстановителем могут быть атом, ион и вещества:
- простые или сложные;
- неорганические или органические;
- газ, жидкость, твердое (расплав).
Окислительное число
В химии существует такое понятие, как степень окисления, также называемое окислительным числом. Это условная величина, она оценивает активность атома при окислении или восстановлении. Эта величина используется для описания свойств соединений или ионов, помогает правильно написать уравнение хим. реакции, составить формулу вещества. Она применяется для указания количества передаваемых или принимаемых электронов.
Обращая внимание на окислительное число, нужно помнить, что это не заряд атома!
Окислительное число определяется по числу электронов, которые нужно добавить иону с положительным зарядом, чтобы атом стал нейтральным, или числу электронов, которые нужно отнять у иона с отрицательным зарядом, чтобы он стал нейтральным.
Самое большое окислительное число +7. Ион +7 проявляет исключительно сильные окислительные свойства и нуждается в семи электронах, чтобы стать нейтральным. Пример вещества с окислительным числом +7 — марганец в перманганате калия.
Наименьшее окислительное число -8. Такой ион проявляет только восстановительные свойства и должен отсоединить восемь электронов, чтобы стать нейтральным.
Окислительное число на письме указывают числовым индексом со знаком над символом элемента. Для того, чтобы не перепутать степень окисления с зарядом, у окислительного числа знак ставится перед числом, а у заряда — после. Кроме этого, заряд ставится не над элементом, а в правом верхнем углу:
-3+1 +6-2
(NH4)2SO4 — формула вещества с окислительными числами элементов;
(NH_4^(1+)) 2 SO_4^(2-) — формула вещества с указанием зарядов ионов.
К популярным окислителям относятся кислород и озон, галогены (F, Br, Cl, I), пероксиды, гипохлориты, хлораты, азотная, серная и селеновая кислота, «царская водка», хром (VI), дихромат калия, перманганаты, атомарный водород, фториды, оксиды и хлориды неметаллов и переходных металлов.
Сильные восстановители это щелочные и щелочноземельные металлы, углерод, кремний, аммиак, аммиачные растворы щелочных и щелочноземельных металлов, гидриды металлов, молекулярный водород.
Существует множество веществ, обладающих свойствами и окислителя, и восстановителя. Они содержат молекулы со средними значениями окислительного числа; могут и отсоединять, и присоединять электроны. Будут они отдавать или принимать электроны — зависит от того, с чем взаимодействуют, например, вода при контакте со фтором восстановитель, а с железом — окислитель.
Применение
Окислители используются:
- для выделения металлов из сульфидных руд;
- при очистке металлов и сплавов от примесей;
- в химпроме в органических и неорганических синтезах;
- при сжигании органического топлива;
- для производства жидкого ракетного топлива и взрывчатых веществ;
- в процессах отбеливания натуральных нитей и тканей, целлюлозы, бумаги;
- для травления металлов;
- для изготовления катодов химических источников тока.
Восстановители востребованы: 
- в металлургии для получения железа из руды;
- при металлотермическом производстве цветных металлов;
- для выделения цветных металлов из водных солевых растворов;
- при получении металлов и их соединений из газов;
- в различных химических реакциях, в органическом синтезе;
- в фотоделе в качестве проявителей;
- для изготовления анодов химических источников тока.
pcgroup.ru