причины, симптомы, диагностика и лечение
Парааутизм – это психогенная форма аутизма, возникающая у детей на основе психической депривации в ранние периоды онтогенеза. Проявляется нарушением коммуникативных функций – обеднением либо полным отказом от общения, замкнутостью, уходом в себя. Имеет место задержка умственного и речевого развития, эмоциональная незрелость в виде аффективных вспышек. Формируется дефицитарность личностной сферы – недоразвитость социальных функций, слабая волевая активность. Основные методы диагностики – клиническая беседа, наблюдение, опрос родителей или воспитателей. Лечение включает психокоррекционные занятия, фармакотерапию транквилизаторами, седативными препаратами.
Общие сведения
Аутизм – расстройство развития, характеризующееся нарушением социальных связей и коммуникативной сферы, аномальным поведением со стереотипиями. Приставка «пара-» указывает на клиническую схожесть парааутизма с истинным аутизмом. При этом существует разница в этиопатогенетических механизмах двух заболеваний. Международная классификация болезней МКБ-10 не имеет диагноза, полностью соответствующего проявлениям психогенного парааутизма, симптоматика наиболее полно описывается в рубрике «Реактивное расстройство привязанности в детском возрасте». Пик диагностики приходится на возраст до 5 лет, распространенность примерно одинакова среди мальчиков и девочек.
Парааутизм
Причины парааутизма
Парааутические расстройства возникают в результате воздействия факторов ближайшей микросоциальной среды. Ведущим и наиболее исследованным из них является психическая депривация – лишение ребенка стимуляции, необходимой для социального развития. На этом основании выделяют пять причин развития парааутизма:
- Нарушение взаимоотношений «мать-дитя». Расстройство обусловлено недостатком эмоциональной близости между ребенком и мамой. Данная причина характерна для неблагополучных семей, в которых матери страдают алкоголизмом, наркоманией, психическими расстройствами.
- Истинное сиротство. В ситуации выраженной социальной депривации оказываются сироты, брошенные дети, беспризорники. В госпиталях, домах малютки и приютах воспитанники зачастую не получают достаточного общения.
- Сенсорная депривация. Нехватка общения бывает основана на органических патологиях с нарушениями работы анализаторных систем. К этой категории относится слепота, глухота, гипокинезия при ДЦП.
- Когнитивная депривация. Причиной парааутизма может выступать продолжительный «информационный голод». Расстройство развивается у малышей и детей постарше, находящихся в насильственной изоляции (удерживание родителями в подвалах, закрытых комнатах), а также воспитанных животными в условиях дикой природы (синдром Маугли).
- Длительная ситуация угрозы. Замкнутость ребенка возникает как реакция психологической защиты при перманентном воздействии опасных для жизни факторов. Примеры таких ситуаций: регулярное физическое насилие в семье, проживание в эпицентре военного конфликта.
Патогенез
Ведущая роль в онтогенезе психики принадлежит процессу формирования и проявления социальных потребностей, превалирующих над потребностями в пище и тепле. При этом удовлетворение физиологических нужд снимает отрицательные эмоции, служит почвой для положительного опыта общения. В основе базовой социальной активности лежит ориентировочный инстинкт, трансформирующийся в потребность свободы, познавательную активность и чувственный голод – функции, представляющие фундамент для инициирования общения. Проблемы первичной социализации, основанные на депривации, провоцируют деформацию психического развития с доминированием искажений сферы общения.
При парааутизме существуют определенные точки приложения повреждающего фактора (депривационные воздействия) на подкорковые структуры и третичные зоны коры головного мозга. Из-за блокады сенсорных фильтров и наличия чувствительной гиперпатии аутистические поведенческие симптомы развиваются по механизму защиты. Как результат обеднения стимуляции средовыми раздражителями отстают в развитии фронтальная и теменная области. На уровне биохимических процессов определяется избыточная активность серотонина, недостаточность окситоцина.
Симптомы парааутизма
Признаки дизонтогенеза при парааутическом расстройстве у младенцев представлены обеднением эмоциональных ответов на речь взрослого, вид незнакомых людей, новую обстановку, яркие игрушки. Годовалые малыши неактивны и безучастны к попыткам общения. У них не формируется ориентировочный рефлекс при оклике, назывании имени. Не проявляется интерес к играм, слушанию песен, сказок, колыбельных, рассматриванию сюжетных картинок. Отсутствует любопытство и страх при смене окружающих людей, нахождении в шумном помещении. Дети одинаково равнодушно относятся к живым и неживым объектам: не радуются игре с домашними питомцами, не улыбаются при виде вкусной еды. Повторная чувственная стимуляция провоцирует бедный ориентировочный ответ – глазное слежение, реже возникают речевые или двигательные реакции.
В раннем детстве сохраняется задержка мимических, жестикуляторных, звуковых и общих моторных реакций. Характерно равнодушное выражение лица, «тусклость» взгляда, однообразие и вялость поз. Дети предпочитают оставаться в одиночестве. Их игры однообразны, состоят из манипулятивных действий: малыши много раз подряд собирают и разбирают пирамидку, складывают карандаши в коробку и вновь достают их, катают машинку по прямой линии вперед и назад, без определенного маршрута. Нет речевых комментариев и звукоподражания. Побудительные игровые мотивы быстро иссякают, отсутствует стремление играть с другими детьми. Периодически наблюдаются регрессивные двигательные комплексы: сосание пальцев, раскачивание туловища, стучание кубиком об пол или поверхность мебели. В периоды бездействия дети становятся отрешенными, застывают неподвижно с «пустым», рассеянным взглядом. Реже наблюдается бесцельная моторная активность – бег по кругу, прыжки.
В динамике развития детей симптомы парааутистического расстройства постепенно изменяются. У дошкольников позже возникает речь и сюжетно-ролевая игра, но в целом способности к общению расширяются. В 6-8 лет на первый план выходят личностные деформации такие как аффективная незрелость (инфантильность) и переживание своей ущербности. Имеются трудности установления дружеских контактов со сверстниками и уважительных отношений со взрослыми. Остаются недоразвитыми социальные эмоции – дети неспособны проявлять сочувствие, соучастие, сопереживание. Проявления ЗПР постепенно редуцируются, достигая пограничного уровня.
Осложнения
При длительном течении и отсутствии медико-психологической помощи парааутизм провоцирует развитие широкого круга невротических симптомов, преимущественно соматизированных. С гораздо большей частотой, чем в общей популяции, возникают простудные заболевания с осложнениями, диатезы, нейродермиты, экземы, энурезы, ночные кошмары. Дети склонны к депрессивным расстройствам, часто находятся в подавленном настроении, плаксивы. Депрессии носят преимущественно астенический и адинамический характер, являются дополнительным провоцирующим фактором для дефицитарного искаженного эмоционально-личностного развития. Формируется стойкое преобладание и постепенное утяжеление дефицитарности волевых, эмоциональных и когнитивных функций.
Диагностика
Основными методами обследования детей с подозрением на парааутизм являются наблюдение и беседа. Диагностика проводится врачом-психиатром. Он оценивает поведенческие и эмоциональные реакции ребенка, выявляет наличие стереотипий, аффективной отстраненности, отсутствие или слабость ориентировочной деятельности. Во время беседы специалист отмечает его заинтересованность общением, способность отвечать на вопросы, удерживать визуальный контакт. Дополнительные данные о симптомах расстройства психиатр получает в ходе опроса родителей либо медицинских и социальных работников, воспитывающих малыша. Дифференциальная диагностика включает различение парааутизма со следующими заболеваниями:
- Ранний детский аутизм. При парааутистических состояниях глубина аутистического дефекта менее значительна, чем при РДА, сохранена способность к установлению контакта при помощи тактильной стимуляции. Негативизм проявляется ситуационно, у некоторых детей практически отсутствует. Четко выделяются два периода развития расстройства: до 6 лет преобладает отставание в социальном и эмоциональном развитии, после этого возраста формируется дефицитарная личность с обедненной эмоциональностью.
- Эндогенный аутизм. В отличие от аутистических проявлений при шизофрении парааутизм не сопровождается симптомами продуктивного психоза – нет бреда и галлюцинаций. Отсутствует своеобразность мышления, качественные изменения его операциональной стороны.
- Умственная отсталость. Психолог дополнительно проводит исследование когнитивной сферы. При психогенном парааутизме в большей степени нарушается эмоционально-поведенческая сфера, а память, интеллект, речевые навыки, комбинаторика относительно нормально развиты. Даже при наличии симптомов ЗПР сохранена обучаемость – дети способны перенимать опыт, адаптировать его под меняющуюся ситуацию. Отличительная черта речи – направленность внутрь, а не на взаимодействие с собеседником.
- Органические поражения ЦНС. Возможна коморбидность парааутизма и органических неврологических заболеваний. В таких случаях отдельные симптомы дизонтогенеза нивелируются, определяется торпидность личностной структуры, признаки задержки умственного развития более тотальны, нередки дисфорические расстройства настроения, неврологическая симптоматика.
Лечение парааутизма
Основные направления помощи больным детям – психокоррекционная работа и медикаментозное лечение. Развивающие занятия проводят клинические психологи и дефектологи. Ключевой принцип организации коррекционного воздействия заключается в максимальном насыщении среды активизирующими факторами, воздействующими на сенсорный, когнитивный и эмоциональный компонент психики ребенка. Для вовлечения маленького пациента во взаимодействие используются разноцветные игрушки, которые трансформируются, воспроизводят звук, вибрации, свет и требуют совместного использования со взрослым.
Специалисты работают через тактильный канал коммуникации (наиболее развитый): усиливают познавательную активность с помощью массажа, разнообразного по текстуре стимульного материала. При выраженных эмоциональных нарушениях детский психиатр назначает прием седативных средств, транквилизаторов, антидепрессантов; при неустойчивости поведения используются небольшие дозы нейролептиков.
Прогноз и профилактика
Парааутизм относится к функциональным обратимым расстройствам развития, поэтому при правильно проводимой психокоррекции его прогноз благоприятный. Если условия воспитания нормализованы до 3-х летнего возраста, то симптомы редуцируются полностью. В более позднем возрасте требуется больше времени и усилий специалистов. Патологические проявления сглаживаются, позволяя ребенку адаптироваться в обществе, но отдельные искажения личности могут сохраняться на протяжении всей жизни. Профилактика парааутизма – создание активной развивающей среды и обеспечение полноценного эмоционального общения с малышом. Одной из таких мер является введение в детских домах практики гостевого режима, при котором одни и те же люди регулярно проводят с ребенком время на выходных – играют, гуляют, посещают культурные и спортивные мероприятия.
www.krasotaimedicina.ru
Когнитивные и эмоционально-аффективные нарушения при дисциркуляторной энцефалопатии | Яхно Н.Н., Захаров В.В.
ММА имени И.М. Сеченова
Психические расстройства, прежде всего когнитивные и эмоциональные нарушения, являются одним из наиболее частых проявлений органических заболеваний головного мозга. В тех случаях, когда нарушения памяти и других когнитивных функций выражены настолько, что препятствуют осуществлению профессиональной и социальной деятельности в прежнем объеме и качестве, принято говорить о деменции. Особенно часто деменция отмечается в пожилом возрасте. Согласно популяционным исследованиям от 5 до 20% пожилых лиц имеют деменцию. Деменция и преддементные когнитивные расстройства регулярно сочетаются с эмоциональными нарушениями, прежде всего в виде депрессивных и тревожно-депрессивных расстройств [22].
Безусловными лидерами в списке причин деменции у пожилых являются болезнь Альцгеймера и сосудистая мозговая недостаточность. Хронические прогрессирующие формы церебральной недостаточности сосудистой этиологии традиционно обозначаются в отечественной литературе термином дисциркуляторная энцефалопатия (ДЭ) [15]. Патогенез ДЭ является весьма сложным и связан как с хронической гипоперфузией головного мозга, так и с повторными острыми нарушениями мозгового кровообращения, а также, в ряде случаев – с ликвородинамическими нарушениями и вторичным нейродегенеративным процессом [3–5,29,34].
«Феномен разобщения» в патогенезе психических нарушений при ДЭ
Ведущую роль в формировании когнитивной недостаточности при ДЭ играет поражение глубинных отделов белого вещества головного мозга и базальных ганглиев, что приводит к нарушению связи лобных головного мозга и подкорковых структур (феномен разобщения). Механизм формирования разобщения связывается в первую очередь с артериальной гипертензией и представляется следующим. Хроническая неконтролируемая артериальная гипертензия приводит к вторичным изменениям сосудистой стенки – липогиалинозу, который развивается преимущественно в сосудах микроциркуляторного русла. Развивающийся вследствие этого артериолосклероз приводит к изменению физиологической реактивности сосудов. В этих условиях снижение кровяного давления в результате присоединения сердечной недостаточности со снижением сердечного выброса или в результате избыточной гипотензивной терапии, или в результате физиологических циркадных изменений кровяного давления приводит к возникновению гипоперфузии в зонах терминального кровообращения. К последним относятся указанные выше глубинные церебральные структуры [9,23,26,37].
Острые ишемические эпизоды в бассейне глубоких пенетрирующих артерий приводят к возникновению небольших по диаметру лакунарных инфарктов в глубинных отделах головного мозга. При неблагоприятном течении артериальной гипертензии повторные острые эпизоды приводят к возникновению т.н. лакунарного состояния, которое является одним из вариантов мультиинфарктной сосудистой деменции [25,29]. Помимо повторных острых нарушений, предполагается и наличие хронической ишемии в зонах терминального кровообращения. Маркером последней является резрежение перивентрикулярного или субкортикального белого вещества – лейкоареозис, который патоморфологически представляет собой зону демиелинизации, глиоз и расширение периваскулярных пространств [9,23,26,32]. В некоторых случаях неблагоприятного течения артериальной гипертензии возможно подострое развитие диффузного поражения белого вещества головного мозга с клиникой быстро прогрессирующей деменции и других проявлениях разобщения, что иногда обозначается в литературе термином
Нейропсихологические проявления «феномена разобщения»
Ведущую роль в формировании когнитивных нарушений при сосудистой мозговой недостаточности играет разобщение лобных долей и подкорковых образований, что приводит к возникновение вторичной дисфункции лобных долей головного мозга. Лобные доли имеют очень существенное значение в когнитивной деятельности. Согласно теории А.Р. Лурия, которая разделяется в настоящее время подавляющим большинством нейропсихологов, лобные доли отвечают за регуляцию произвольной деятельности: формирование мотивации, выбор цели деятельности, построение программы и контроль за ее достижением [10–12]. При этом дорзолатеральная лобная доля коры и ее связи с стриарным комплексом обеспечивают переключаемость внимания, что необходимо для смены алгоритма деятельности. Орбитофронтальные отделы участвуют в подавлении нерелевантных цели побуждений, обеспечивая таким образом устойчивость внимания и адекватность поведенческих реакций. Кроме того, орбитофронтальная лобная кора находится в тесной взаимосвязи с гиппокампом, обеспечивая устойчивость внимания в мнестической деятельности [13,37].
Дисфункция лобных долей головного мозга приводит к формированию дизрегуляторного синдрома. При этом сохраняются операциональные механизмы памяти, восприятия, двигательные и языковые навыки, но нарушается программирование деятельности: развивается патологическая инертность, связанная с недостаточностью переключаемости внимания либо, напротив, избыточная импульсивность вследствие неустойчивости произвольного внимания, либо различные их сочетания [10–12].
Другие патогенетические механизмы когнитивных нарушений
Помимо поражения глубинных церебральных структур и возникновения феномена разобщения со вторичной дисфункцией лобных отделов головного мозга, в патогенезе когнитивных нарушений несомненную роль играют инфаркты мозга корковой локализации. Стратегически важными для когнитивной деятельности являются ассоциативные зоны лобной коры и зоны стыка теменно-височно-затылочной коры, а также структуры гиппокампового круга. В некоторых случаях возможно возникновение постинсультной деменции, связанной с перенесенным единичным крупноочаговым инфарктом мозга стратегической локализации [4, 32, 40].
Не менее важным аспектом патогенеза когнитивных расстройств при ДЭ является присоединение нейродегенеративного процесса. Согласно патоморфологическим данным, сосуществование сосудистых изменений и маркеров нейродегенерации альцгеймеровского характера (сенильные амилоидные бляшки, нейрофибриллярные внутриклеточные сплетения, апоптоз нейронов медибазальных лобых отделов, гиппокампа и височно-теменных долей головного мозга) не является редким. В этих случаях принято говорить о смешанном сосудисто-дегенеративном характере деменции. Частота встречаемости смешанной деменции значительно превосходит ожидаемую при случайном совпадении двух болезней. Этот факт имеет теоретическое объяснение: гипоксия является фактором, ускоряющим нейродегенеративные изменения, причем особенно чувствительны к гипоксии нейроны гиппокампа [27]. Поэтому, сосудистая мозговая недостаточность расценивается в настоящее время как фактор риска и один из патогенетических механизмов развития болезни Альцгеймера. Таким образом, по крайней мере у части больных существенный вклад в развитие когнитивных расстройств вносит сопутствующий дегенеративный процесс [34, 36].
Патогенез эмоциональных нарушений при ДЭ
Достаточно сложным и разнородным представляется патогенез депрессивных симптомов при ДЭ и их взаимосвязь с когнитивными расстройствами. Во–первых, эмоциональные нарушения, как и когнитивные, могут быть результатом вторичной дисфункции лобных отделов головного мозга. Известно, что связи дорзолатеральной лобной коры и стриарного комплекса участвуют в формировании положительного эмоционального подкрепления при достижении цели деятельности. Нарушение этих связей в результате феномена разобщения будет приводить к недостаточности положительного подкрепления и, как следствие, к хронической фрустрации, что является предпосылкой возникновения депрессии [13, 38].
Депрессивные симптомы регулярно описываются при поражении лобных долей головного мозга различной этиологии [13]. Однако следует иметь в виду, что некоторые проявления лобной дисфункции могут имитировать депрессию в отсутствие истинного снижения фона настроения. Речь идет о мотивационных расстройствах вследствие нарушения связей цингулярной извилины и лимбической системы. Хорошо известна также неустойчивость внешнего аффекта, что связанно с избыточной подвижностью произвольного внимания и снижением критики в результате дисфункции орбитофронтальной коры [10–13, 45].
Наряду с биологическими предпосылками депрессии при лобной дисфункции, несомненную роль играют также психогенные факторы. Безусловно, переживание своей нарастающей интеллектуальной и, как правило, двигательной неспособности вносит свой вклад в формирование депрессивных расстройств, по крайней мере, на ранней стадии деменции, в отсутствие выраженного снижения критики.
Наличие эмоциональных нарушений способно усугублять выраженность когнитивных расстройств из–за повышения уровня тревоги и связанных с этим трудностей сосредоточиться, неуверенности и ожидания неудачи. Таким образом, взаимосвязи когнитивных и эмоциональных нарушений достаточно сложны. Оба вида психических расстройств связаны наличием общих патогенетических факторов (феномен разобщения и лобная дисфункция), а также способны непосредственно влиять друг на друга по описанным выше психологическим механизмам [16].
Клинические характеристики когнитивных нарушений при ДЭ
Поскольку патогенез когнитивных расстройств при ДЭ гетерогенен, клинические проявления интеллектуального дефицита также неоднородны. Однако ведущим в большинстве случаев является синдром «подкорковой» деменции или преддементных когнитивных расстройтсв. Патогенез данного вида когнитивных нарушений связан с поражением глубинных отделов белого и серого вещества головного мозга по указанным выше патологическим механизмам.
Термин «подкорковая» деменция был впервые предложен M. Albert и соавт. в 1974 для обозначения когнитивных расстройств при прогрессирующем надъядерном параличе [21]. В дальнейшем, аналогичные когнитивные расстройства описывались и при других неврологических заболеваниях: болезни Паркинсона, сосудистой деменции, рассеянном склерозе и других поражениях глубинных церебральных структур. Сам термин не вполне удачен, поскольку важную роль в патогенезе «подкорковых» когнитивных расстройств играет дисфункция лобной коры. Тем не менее, этот термин состоялся с клинической точки зрения и широко применяется в литературе [26,40,49].
Подкорковая деменция характеризуется прежде всего замедленностью умственной деятельности – брадифренией: больному требуется больше, чем в норме, времени и попыток для того, чтобы решать насущные интеллектуальные задачи. Отмечается недостаточность кратковременной памяти при относительной сохранности долговременной. Такое своебразие мнестических расстройств обусловливает сохранность памяти о событиях жизни при выраженных затруднениях в обучении, при одновременной работе с несколькими источниками информации и при решении многоэтапных задач, требующих сохранности памяти о промежуточном результате деятельности. «Подкорковая» деменция характеризуется также нарушением восприятия и моторного выражения пространственных отношений, что проявляется при конструировании и в рисунке. Интеллектульная сфера характеризуется нарушением обобщений в результате недооценки условий задания и принятия импульсивных решений. В отличие от болезни Альцгеймера и локальных поражений коры головного мозга, для «подкорковых» деменций не характерны амнезия на текущие событий, апраксия, агнозия и афазия [13,21,26,40,49].
Описания когнитивных нарушений при ДЭ и сосудистой деменции в целом соответствуют упомянутой выше модели «подкорковых» деменций. Однако наличие церебральных инфарктов корковой локализации или сопутствующего нейродегенеративного процесса могут весьма модифицировать клиническую картину, добавляя в нее признаки, характерные для первичного поражения височно-теменных отделов головного мозга. Сопутствующий нейродегенеративный процесс, как правило, возникает у лиц более пожилого возраста. Клиническая картина когнитивных расстройств при этом может в большей степени напоминать болезнь Альцгеймера [3,4,13,16,18,41,49].
Клинические особенности эмоциональных нарушений при ДЭ
Наиболее типичным изменением эмоционального состояния при ДЭ является развитие депрессии. Однако, как правило, выраженность депрессивных расстройств не достигает степени большого депрессивного эпизода по критериям DSM–IV. На ранних стадиях заболевания депрессия при ДЭ носит ипохондрические черты. Выраженность ипохондрии, однако, уменьшается по мере прогрессирования сосудистой мозговой недостаточности. Тяжесть депрессивных симптомов при ДЭ зависит от стадии заболевания и выраженности неврологических нарушений. Имеется также связь с выраженностью когнитивных расстройств и наличием деменции: при этом отмечается большая выраженность депрессии [16].
Весьма любопытны данные о клинико-нейровизуализационных сопоставлениях. В работе Т.А. Янакаевой было показано, что наличие и тяжесть симптомов депрессии зависят от выраженности очаговых изменений белого вещества лобных долей головного мозга и нейровизуализационных признаков ишемического повреждения базальных ганглиев. Эти наблюдения свидетельствуют о биологической природе депрессии при ДЭ, вероятно, связанной главным образом с феноменом лобно-подкоркового разобщения [16].
Диагноз и дифференциальный диагноз сосудистой деменции
В дифференциальном диагнозе сосудистой и первично-дегенеративной деменции весьма важную роль играет сочетание когнитивных нарушений и других клинических проявлений феномена разобщения. К последним относятся псевдобульбарный синдром, олигобрадикинезия, апраксия ходьбы, постуральные и тазовые расстройства. В типичных случаях когнитивные расстройства подкоркового характера и симптомы депрессии в сочетании с вышеуказанными неврологическими нарушениями отмечаются у пожилого пациента с историей повоторных инсультов и длительно существующего сосудистого заболевания, например, гипертонической болезни или церебрального атеросклероза [3,17,18,35].
Важную роль в верификации сосудистой природы когнитивных и эмоциональных нарушений играют методы нейровизуализации: КТ и МРТ головного мозга. В настоящее время диагноз сосудистой деменции считается неправомерным без нейровизуализационного подтверждения. Типичными находками для ДЭ являются очаговые и диффузные изменения белого вещества, постишемические кисты и церебральная атрофия. По некоторым данным, выраженность изменений белого вещества коррелирует с выраженностью когнитивных и эмоциональных нарушений при ДЭ [3,9,17,18].
Фармакотерапия психических нарушений при ДЭ
Лечение когнитивных и эмоциональных нарушений при ДЭ должно быть, по возможности, этиотропным или патогенентическим. Поскольку в основе психических нарушений равно как и других симптомов ДЭ лежит сосудистое заболевание головного мозга, первоочередная задача врача – коррекция факторов риска инсульта и устранение или уменьшение выраженности хронической ишемии головного мозга. Лечение артериальной гипертензии, назначение антиагрегантов, хирургическая коррекция атеросклеротического сужения магистральных артерий, несомненно, способствует профилактике нарастания когнитивых расстройств и, по некоторым данным, уменьшению выраженности имеющегося когнитивного дефекта. Важное значение имеет также контроль гиперлипидемии, гипергликемии, лечение других соматических заболеваний [7].
Патогенетически обосновано применение препаратов с вазоактивными, нейропротективными и метаболическими свойствами. Вазоактивные препараты улучшают церебральную микроциркуляцию, воздействуя на тонус артериол и реологические свойства крови. Широко применяются на практике такие препараты, как танакан, винпоцетин, пентоксифиллин, вазобрал, блокаторы кальциевых каналов (нимодипин, циннаризин, флунаризин и др.). Данные препараты обладают способностью уменьшать выраженность когнитивных расстройств при ДЭ. При этом, как правило, наибольший эффект отмечается в наиболее подвижных когнитивных сферах, таких как напряженность внимания и память [7].
Цель применения нейропротективных препаратов – улучшить выживаемость нейронов в условиях хронической ишемии и гипоксии, что способствует вторичной профилактике нарастания выраженности когнитивных и других неврологических расстройств. Учитывая важную патогенетическую роль процессов перекисного окисления липидов в ишемическом повреждении, нейропротективным действием могут обладать препараты с антиоксидантными свойствами. Oбсуждается вероятный антиоксидантный эффект селегелина, токоферола и танакана. Наибольший клинический опыт применения при ДЭ имеется в отношении танакана, который сочетает в себе как вазоактивные, так и нейропротективные свойства. Данный препарат в ряде исследований показал способность уменьшать выраженность когнитивных, эмоциональных и субъективных симптомов ДЭ. Однако способность танакана модифицировать течение заболевания нуждается в дополнительном изучении [8,19,28,31].
Нейропротективным потенциалом обладают также препараты, уменьшающие содержание внутриклеточного кальция в нейронах, такие как нимодипин, поскольку накопление кальция усиливает энергетические процессы и способствует гибели нейронов. Симптоматический ноотропный эффект и потенциальная возможность модифицировать течение заболевания описывается также у блокатора NMDA-рецепторов акатинола мемантина [7,36].
Нейрометаболическая терапия применяется с симптоматической целью для уменьшения выраженности когнитивных и других неврологических нарушений. Кроме того, по некоторым данным, метаболическая терапия обладает возможностью модифицировать течение заболевания. Классом препаратов, специально синтезированных для применения в качестве ноотропных средств, являются ГАМК-ергические препараты: пирацетам и его модификации. Эффективность терапии во многом зависит от режима дозирования. Более целесообразно внутривенное применение в достаточно высоких дозировках [7].
В качестве нейрометаболической терапии хорошо зарекомендовал себя пептидэргический препарат церебролизин. Церебролизин содержит свободные аминокислоты и полипептиды, которые как показывают экспериментальные наблюдения, обладают нейротрофическим эффектом [2,6]. Показано, что церебролизин при внутривенном введении в дозах 15–30 мл оказывает благоприятное действие, главным образом, на когнитивные функции, способствуя улучшению концентрации внимания, мнестических функций и интеллектуальных процессов [1,14,20,35,39].
В качестве ноотропных препаратов используются ацетилхолинергические препараты, учитывая роль ацетилхолинергической медиации в процессах внимания и памяти. В настоящее время доказано, что ингибиторы ацетилхолинэстеразы, такие как ривастигмин и амиридин, улучшают когнитивные функции при деменции альцгеймеровского типа. При ДЭ и сосудистой деменции эти препараты целесообразно назначать при смешанном характере деменции с наличием сопутствующего дегенеративного процесса. Следует отметить, что ингибиторы ацетилхолинэстеразы могут усиливать выраженность депрессии. Поэтому при сочетании когнитивных и эмоциональных расстройств лечение следует начинать с коррекции симптомов депрессии. С целью усиления ацетилхолинергической медиации как при болезни Альцгеймера, так и при сосудистой деменции также используется предшественник ацетилхолина глиатилин [7, 36].
В психофармакотерапии депрессии, связанной с сосудистой мозговой недостаточностью, предпочтительнее назначение препаратов с минимальным холинолитическим эффектом, поскольку последний может способствовать усугублению тяжести когнитивных расстройств. Наиболее целесообразно применение селективных блокаторов обратного захвата серотонина, таких как флуоксетин [36]. Легкий антидепрессивный эффект при сосудистой моговой недостаточности описывается также у танакана, который может применяться при нетяжелой симптоматической депрессии, связанной с ДЭ [31].
Заключение
Таким образом, когнитивные и эмоциональные нарушения являются закономерной составной частью клинической картины дисциркуляторной энцефалопатии. В основе психических расстройств при ДЭ лежит поражение глубинных отделов полушарий головного мозга (базальных ганглиев и глубинных отделов белого вещества), связанное как с хронической гипоперфузией, так и с повторными острыми нарушениями мозгового кровообращения. Поражение глубинных церебральных отделов ведет к разобщению связей лобных отделов и подкорковых структур, что и приводит к возникновению вторичной дисфункции лобных долей головного мозга, проявлением которой являются когнитивные расстройства «подкорково-лобного» характера и симптомы депрессии. Лечение психических расстройств сосудистой этиологии должно включать как лечение основного сосудистого заболевания, так и вазоактивные, нейропротективные и метаболические препараты.
Литература:
1. Верещагин Н.В., Лебедева Н.В. Легкие формы мультиинфарктной деменции: эффективность церебролизина. //Сов.Медицина.-1991.-N.11. –c.6–8.
2. Виндиш М. Церебролизин – новейшие результаты, подтверждающие разностороннее действие лекарства.// В кн.: Третий Международный Симпозиум по Церебролизину. –1991. Москва. –С.81–106.
3. Дамулин И.В. Дисциркуляторная энцефалопатия в пожилом и старческом возрасте. //Автореферат дисс… докт.мед.наук. –М. –1997. –С.32.
4. Дамулин И.В. Сосудистая деменция. //Неврологический Ж. –1999. –Т.3. -№.4. –С.4–11.
5. Дамулин И.В., Орышич Н.А., Иванова Е.А. Нормотензивная гидроцефалия. //Неврол. Ж. –1999. –Т.4. -№.6.-С.51–56.
6. Дамулин И.В., Захаров В.В., Левин О.С., Елкин М.Н. Использование церебролизина в нейрогериатрической практике. //В сб.: Н.Н.Яхно, И.В.Дамулин (ред): Достижения в нейрогериатрии. –Москва, 1995. –Ч.1. –С.100–115.
7. Захаров В.В., Дамулин И.В., Яхно Н.Н. Медикаментозная терапия деменций. Клиническая фармакология и терапия. –1994. –Т.3. -№ 4. –С.69–75.
8. Захаров В.В., Яхно Н.Н. Применение танакана при нарушении мозгового и периферического кровообращения. //Русский Медицинский Журнал. –2001. –Т.9. -№ 15. –С.645–649.
9. Левин О.С., Дамулин И.В. Диффузные изменения белого вещества (лейкоареоз) и проблема сосудистойй деменции. //В кн. под ред. Н.Н.Яхно, И.В.Дамулина: Достижения в нейрогериатрии. –1995. –Ч.2. –С.189–231.
10. Лурия А.Р. Высшие корковые функции человека. Изд.2. –Москва : издательство МГУ, 1969 г.
11. Лурия А.Р. Основы нейропсихологии. –Москва : издательство МГУ, 1973.
12. Лурия.А.Р. Лобные доли и регуляция психических процессов. –М., Изд-во Московского Университета, 1966.
13. Пилипонич А.А., Захаров В.В., Дамулин И.В. Лобная дисфункция при сосудистой деменции. //Клиническая геронтология. –2001. –Т.5. -№ 6. –С.35–41.
14. Соловьев О.И. Нейротропное действие церебролизина по данным компьютеризированной топографии и визуального анализа ЭЭГ. //В кн.: Третий Международный Симпозиум по Церебролизину. –1991. Москва.-с.61–70.
15. Шмидт Е.В. Классификация сосудистых поражений головного испинного мозга. //Ж. Невропатологии и Психиатрии. –1985. –Т.85. –С.192–203.
16. Янакаева Т.А. Эмоционально-аффективные нарушения при дисциркуляторной энцефалопатии и болезни Паркинсона. //Автореферат дисс… канд.мед.наук. –М. –1999.
17. Яхно Н.Н., Левин О.С., Дамулин И.В. Сопоставление клинических и МРТ-данных при дисциркуляторной энцефалопатии. Сообщение 1: двигательные нарушения. //Неврол. Ж. –2001. –Т.6. -№.2. –С.10–16.
18. Яхно Н.Н., Левин О.С., Дамулин И.В. Сопоставление клинических и МРТ-данных при дисциркуляторной энцефалопатии. Сообщение 2: когнитивные нарушения. //Неврол. Ж. –2001. –Т.6. -№.3. –С.10–19.
19. Яхно Н.Н., Дамулин И.В., Захаров В.В., Елкин М.Н., Ерохина Л.Г., Стаховская П.В., Чекнева Н.С., Суслина З.А., Тимербаева С.Л., Федин П.А., Бодарева Э.А., Скоромец А.А., Сорокоумов В.А., Ивашкин В.Т., Григорьев Ю.В., Первозванский Б.Е. Применение танакана при начальных стадиях сосудистой мозговой недостаточности: результаты открытого многоцентрового исследования. //Неврологический журнал. –1998. –Т.3. -№.6. –С.18–22.
20. Яхно Н.Н., Дамулин И.В., Захаров В.В., Левин О.С., Елкин М.Н. Опыт применения высоких доз церебролизина при сосудистой деменции. Тер Архив. –1996. –Т.68. -№ 10. –С.65–69.
21. Albert M.L. Subcortical dementia. In: Alzheimer’s disease : Senile Dementia and Related Disorders. –New York, Raven Press, 1978, V.7, pp 173–180.
22. Amaducci L., Andrea L. The epidemiology of the dementia in Europe. In: A.Culebras, J.Matias Cuiu, G.Roman (eds) : New concepts in vascular dementia . –Barselona : Prous Science Publishers, 1993, pp 19–27.
23. Awad I.A., Masaryk T., Magdinec M. Pathogenesis of subcortical hypertense lesions on MRI of the brain. //Stroke. –1993. –V.24. –P.1339–1346.
24. Cummings J.L., Benson D.F. Subcortical dementia. Review of an emerging concept. //Arch Neurol. –1984. –V.41. –P.874–879.
25. Fisher C.M. Lacunar strokes and infarcts.//Neurology. –1982. –V.32. –P.871–876.
26. Inzitari D., Marinoni M., Ginanneschi A. Pathophysiology of leucoaraiosis. // In: New concepts in vascular dementia. A.Culebras, J.Matias Guiu, G.Roman (eds). Barcelona: Prous Science Publishers. –1993. –P.103–113.
27. Iqbal K., Winblad B., Nishimura T., Takeda M., Wisniewski H.M. (eds) Alzheimer’s Disease: Biology, Diagnosis and Therapeutics John Willey and Sons Ltd, 1997, 830 p.
28. Israel L., Dell’Accio E., Martin G., Hugonot R. Extrait de Ginkgo biloba et expercises d’entrainement de la memoire. Evaluation comparative chez des personnes agees ambulatoires. //Psychol Med. –1987. –V.19. –P.1431–1439.
29. Hachinski V.C., Lassen N.A., Marshall J. Multi–infarct dementia. A case of mental deterioration in the elderly. //Lancet. –1974. –V.2.-P.207–210.
30. Hachinski V.C. Binswanger disease: neither Binswanger’s nor a disease. //J. Neur. Sci. –1991. –V.103. –P.1–13.
31. Halama P. Was leistet der Spezialextrakt (Egb 761) //Therapiewoche. –1990. –V.40. –P.3760–3765.
32. Hershey L.A., Olszewski W.A. Ischemic vascular dementia. //In: Handbook of Demented Illnesses. Ed. by J.C.Morris. –New York etc.: Marcel Dekker, Inc. –1994. –P.335–351
33. Huber S.J., Shuttleworth E.C., Paulson G.W. et al. Cortical vs subcortical dementia: neuropsychological differences. Arch Neurol. –1986. –V.43. –P.392–394.
34. Кalaria R.N., Lewis H., Cookson N.J., Shearman M. The impact of certebrovascular disease on alzheimer’s pathology in elderly. //Neurobiol. aging. –2000. –V.21.-N.1.S.-P.S.66–67.
35. Kofler B., Erhart C., Erhart P. Harrer G. A multi–dimentional approach in testing nootropic drug effects (Cerebrolysin). //Arch. Gerontol. Geriatr. –1990. –V.10. –Р.128–140.
36. Lovenstone S., Gauthier S. Management of dementia. //-Martin Dunitz Ltd. –2000. –P.145.
37. Roman G.V. Vascular dementia: NINDS – AIREN diagnostic criteria. //In: New concepts in vascular dementia. A.Culebras, J.Matias Guiu, G.Roman (eds). Barcelona: Prous Science Publishers. –1993. –P.1–9.
38. Saint–Cyr J.A., Taylor A.E., Nikolson K. Behavior and basal ganglia. //In : W.J.Weiner, A.E.Lang (eds) : «Behavioral Neurology of Movement Disorder». Adv Neurol. –1995. –V.65. –P.1–29.
39. Suchanek–Frohlich H., Wunderlich E. Uber die Wirksamkeit eines Aminosaure– Peptid– Randomisierte Doppelblind– Placebo– Vergleichsstudie. //Neuropsychiatrie. 1986. –V.1. –N.1. –P.45–48.
40. Tien R. The Dementias: Correlation of Clinical Features, Pathophisiology, and Neuroradiology. // A. J. R. –1993. –V.161. –P.245–255.
www.rmj.ru
Фармакотерапия когнитивных нарушений различного генеза: современное состояние и перспективные направления | Ушкалова Е.А., Ушкалова А.В.
Когнитивные расстройства являются самыми распространенными неврологическими симптомами, т. к. практически любое заболевание с вовлечением ЦНС сопровождается их развитием [1].
Причины когнитивных расстройств
Причинами когнитивных расстройств могут быть нейродегенеративные и сосудистые заболевания головного мозга, токсические и дисметаболические энцефалопатии, нейроинфекции и другие патологии (табл. 1). Во многих случаях в основе деменции лежат два и более состояния, наиболее часто – сочетание болезни Альцгеймера (БА) с другой патологией головного мозга [2].
Наблюдающийся в последние десятилетия рост распространенности когнитивных расстройств обусловлен в первую очередь постарением населения [1, 4]. Наиболее распространенным типом деменции у пожилых людей является БА, далее следует деменция с тельцами Леви [5, 6]. «Чистая» сосудистая деменция встречается редко, однако сосудистые заболевания головного мозга, включая субклинические поражения, «немой» инфаркт мозга и клинически явный инсульт, являются важными независимыми факторами, вносящими существенный вклад в ухудшение когнитивной функции у пациентов с другими заболеваниями [2].
Риск развития когнитивных расстройств повышается при ряде соматических патологий, в т. ч. сердечно-сосудистых, сахарном диабете и метаболическом синдроме, дисфункциях щитовидной железы, выраженном поражении функции печени и почек, гиперхолестеринемии и гипергомоцистеинемии, дефиците витаминов группы В, синдроме обструктивного апноэ сна, хроническом обструктивном заболевании легких, анемии и ряде других [5].
Лечение когнитивных расстройств
Лечение когнитивных расстройств, в тех случаях, когда это возможно, в первую очередь должно быть направлено на устранение основной причины. Например, при нейроинфекциях главная роль принадлежит этиотропной терапии, направленной на эрадикацию возбудителя, при артериальной гипертензии – антигипертензивным препаратам, при хронической сосудистой мозговой недостаточности – препаратам, улучшающим микроциркуляцию, при болезни Паркинсона – низким (до 500 мг) дозам леводопы и т. д. [2, 3]. При наличии нескольких патологий лечение должно быть прежде всего направлено на устранение факторов, вносящих наибольший вклад в развитие деменции [2]. Болезнь-модифицирующих препаратов при нейродегенеративных заболеваниях в настоящее время не существует, поэтому в этих случаях проводится симптоматическое и поддерживающее лечение. Среди препаратов для симптоматической терапии наиболее хорошо изучены ингибиторы холинэстеразы (иХЭ) (антихолинэстеразные средства) и мемантин.
Ингибиторы холинэстеразы
Основанием для применения иХЭ послужила «холинергическая гипотеза», согласно которой важным фактором, способствующим снижению когнитивных функций в пожилом возрасте и при БА, является дефицит ацетилхолина в ЦНС, а восстановление его запасов приводит к улучшению когнитивных функций [7]. Эта гипотеза получила подтверждение в экспериментальных и клинических исследованиях.
иХЭ рекомендуют преимущественно пациентам с БА легкой/умеренной степени тяжести. Однако при легких когнитивных расстройствах применение иХЭ, по данным метаанализа, ассоциируется с минимальной пользой, которую следует сопоставлять с риском развития побочных эффектов, особенно желудочно-кишечных [8]. В некоторых странах их применение также одобрено при тяжелой деменции, однако эффективность иХЭ у этих больных подвергается сомнению [5].
Препараты данной группы также улучшают когнитивные функции у пациентов с болезнью Паркинсона и деменцией с тельцами Леви, что подтверждается результатами недавно опубликованного метаанализа 10 РКИ [9]. При деменции с тельцами Леви они также способствуют улучшению поведенческих симптомов [10].
Доказательные данные об эффективности иХЭ при сосудистой деменции ограниченны и противоречивы [11, 12]. В последних канадских рекомендациях, опубликованных в 2014 г., препараты этой группы рекомендованы для лечения деменции с сосудистым компонентом (наиболее распространенным типом деменции смешанного патогенеза), но не «чистой» сосудистой деменции [2]. Убедительных доказательств эффективности иХЭ при ЛВД не получено, более того, есть данные, что они могут ухудшать у этих пациентов поведенческие симптомы [13]. Также нет доказательств эффективности иХЭ при других нейрокогнитивных расстройствах.
Данные о влиянии иХЭ на отдаленные исходы, такие как замедление нарушений повседневного функционирования и удлинение срока до помещения в специализированные учреждения по уходу, противоречивы [14].
иХЭ достаточно часто вызывают побочные эффекты, в частности нежелательные симптомы со стороны ЖКТ (тошнота, рвота, диарея, потеря аппетита, снижение веса) наблюдаются примерно у 10–15% пациентов [3]. Серьезные нежелательные реакции, наиболее часто со стороны ЦНС и ЖКТ, а также сердечные аритмии преимущественно развиваются у больных старческого возраста, а также получающих сопутствующую терапию антипсихотиками первого и второго поколения, антигипертензивными лекарственными средствами и препаратами, влияющими на ЖКТ и обмен веществ [15]. Применение иХЭ ограничивает ряд абсолютных и относительных противопоказаний, в их числе язвенная болезнь желудка и двенадцатиперстной кишки, почечная и печеночная недостаточность, синдром слабости синусового узла, брадикардия, бронхиальная астма и эпилепсия [3].
Мемантин
Мемантин является неконкурентным антагонистом глутаматных NMDA(N-метил-D-аспартат)-рецепторов. Предполагают, что он оказывает нейропротективное действие в отношении эксайтотоксичности в коре больших полушарий и гиппокампе, обусловленной избыточным выбросом глутамата в синаптическую щель [16].
Эффективность мемантина показана у пациентов со среднетяжелой и тяжелой БА, но не при других формах деменции [17]. Помимо влияния на когнитивные функции мемантин вызывает небольшое снижение ажитации у больных с деменцией [18].
У пациентов с деменцией с тельцами Леви и когнитивными нарушениями, ассоциированными с болезнью Паркинсона, мемантин вызывал небольшое улучшение общего состояния (по шкале CGI), но не влиял на когнитивные функции [9]. Есть сообщения об ухудшении симптомов бреда и галлюцинаций при применении мемантина у пациентов с деменцией с тельцами Леви [5].
При легкой и умеренной сосудистой деменции он оказывал небольшой и клинически не значимый эффект [18]. Данные исследований мемантина при ЛВД противоречивы [19].
Достоинством мемантина является его хорошая переносимость [5].
Другие препараты
В систематических обзорах и метаанализах не удалось получить доказательств эффективности при каких-либо деменциях пирацетама [20], мелатонина [21] и витаминов [22–24]. Также не доказана способность статинов, заместительной гормональной терапии и нестероидных противовоспалительных препаратов (НПВП) предотвращать ухудшение когнитивных функций [25]. Более того, в 2012 г. на основании спонтанных сообщений о побочных реакциях FDA (США) внесло в инструкции по применению статинов предостережение о возможном нарушении когнитивных функций при их использовании [26]. В целенаправленном систематическом обзоре не удалось ни подтвердить, ни опровергнуть это предостережение, особенно в отношении высоких доз препаратов [27]. Аналогичные данные имеются для НПВП (рофекоксиба, целекоксиба и напроксена) и эквин-эстрогена [25].
Таким образом, выбор препаратов, улучшающих когнитивные функции, остается крайне ограниченным. Кроме того, эффективность иХЭ и мемантина умеренная, и они позволяют задерживать прогрессирование когнитивных нарушений в среднем лишь на несколько месяцев. При неэффективности монотерапии часто рекомендуют комбинировать иХЭ и мемантин. Эта комбинация представляется безопасной и рациональной, поскольку ее ингредиенты имеют разные механизмы действия, однако доказательных данных для того, чтобы поддержать или отвергнуть ее применение, на сегодняшний день недостаточно [2].
Поиск эффективных препаратов для лечения когнитивных расстройств продолжается, в настоящее время клинические исследования проходят 70 новых препаратов, предназначенных для лечения БА [28]. Внимание исследователей привлекают и «старые» средства, оказывающие благоприятное влияние на когнитивные функции. К их числу относится холина альфосцерат (ХАФ) [29, 30].
Холина альфосцерат и его комбинации с другими препаратами
ХАФ является предшественником ацетилхолина. Он легко проходит через гематоэнцефалический барьер и в головном мозге расщепляется на холин и глицерофосфат [30]. Холин является субстратом для синтеза нейромедиатора ацетилхолина, некоторых сигнальных молекул и липидов, включая необходимые компоненты клеточных мембран (фосфатидилхолин, лизофосфатидилхолин, сфингомиелин), а также донатором метильных групп, необходимых для процессов метилирования ДНК и ресинтеза метионина [31]. Глицерофосфат – предшественник фосфатидилхолина – одного из главных фосфолипидов клеточных мембран, при повреждении которых в результате ишемических процессов в головном мозге образуются высокотоксичные свободные радикалы. Фосфатидилхолин восстанавливает фосфолипидный состав мембран нейронов и улучшает их пластичность.
В экспериментах на животных показано, что ХАФ усиливает выделение ацетилхолина в гиппокампе, улучшает память и обучение, оказывает протективный эффект в отношении микроанатомии головного мозга при экспериментальной модели сосудистой деменции, снижает структурные изменения в головном мозге, обусловленные старением, в т. ч. отвечающие за память и обучение [30–32].
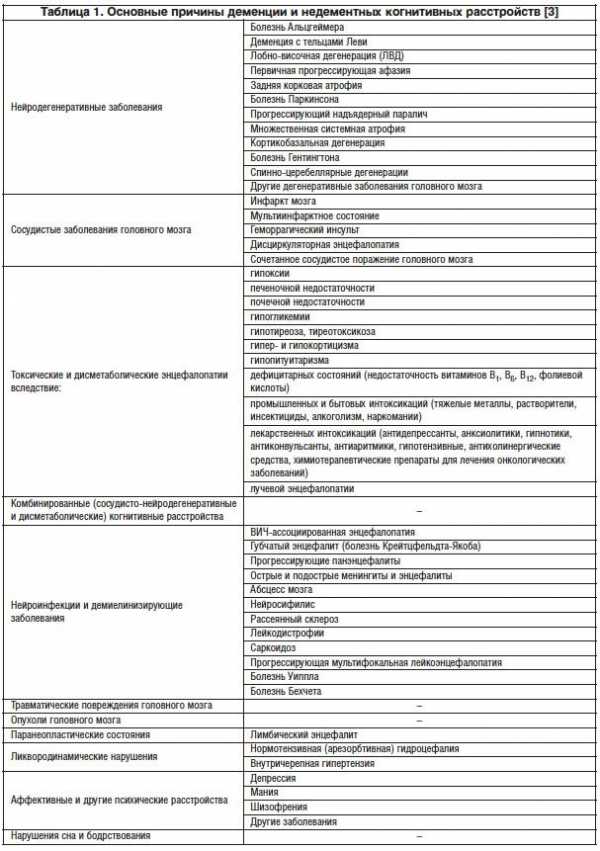
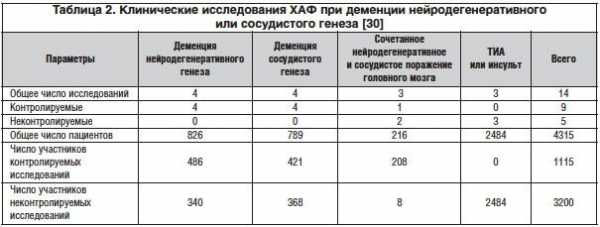
ХАФ изучался в 14 клинических исследованиях с участием 4054 пациентов при деменции нейродегенеративного и сосудистого генеза (табл. 2) и продемонстрировал благоприятное влияние на ориентацию, внимание, память, речь и настроение [32]. В трех из них (n=2484) показана способность ХАФ улучшать функциональное восстановление у пациентов, перенесших инсульт или транзиторную ишемическую атаку (ТИА)[32].
Аналогичные результаты получены в многоцентровом открытом исследовании в Италии, в котором 2044 пациента, недавно перенесших инсульт или ТИА, получали в течение первого месяца инъекции ХАФ, а далее в течение 5 мес. – препарат внутрь [33]. К концу исследования в соответствии с оценкой по шкале Global Deterioration Scale (Шкала общего ухудшения состояния) 71% пациентов соответствовали критериям «отсутствия когнитивного ухудшения». Статистически значимое улучшение было получено и при оценке по всем другим тестам. В исследовании также была продемонстрирована прекрасная переносимость препарата.
Сходные данные были получены и в исследованиях отечественных ученых с применением препарата Церетон (ХАФ) [34–37]. В одном из них с участием 95 пациентов с ишемическим каротидным инсультом показана не только клиническая, но и затратная эффективность Церетона по сравнению со стандартной терапией [37].
При когнитивных расстройствах, ассоциированных с болезнью Паркинсона, Церетон достоверно превосходил по эффективности пирацетам [38]. Кроме того, в отличие от пирацетама, применение которого ассоциировалось с тенденцией к увеличению выраженности психотических нарушений, введение ХАФ сопровождалось уменьшением некоторых поведенческих симптомов, прежде всего апатии, а также с достоверным улучшением качества жизни больных. Улучшение настроения пациентов и устранение эмоциональной лабильности, наряду с улучшением соматического состояния, под влиянием ХАФ у пациентов с когнитивными нарушениями различного генеза также отмечено и в других исследованиях [29, 30].
Включение ХАФ на ранних этапах в состав комплексной терапии приводило к улучшению исходов у пациентов (n=23) с черепно-мозговой травмой [39].
Преимуществом ХАФ перед иХЭ является его безопасность и хорошая переносимость, в т. ч. больными с брадикардией, бронхиальной астмой и другими сопутствующими соматическими заболеваниями, являющимися противопоказанием к применению иХЭ [30, 40]. Хорошая переносимость и благоприятное влияние на соматические симптомы позволили экспертам рассматривать ХАФ в качестве препарата выбора у больных с деменцией различного генеза и степени тяжести старше 85 лет. Препарат показывает коррекцию легких и умеренных когнитивных расстройств, в т. ч. при наличии сосудистой коморбидности и других сопутствующих заболеваниях [30, 32].
Для повышения эффективности терапии когнитивных нарушений ХАФ можно комбинировать с препаратами других групп. В многоцентровом двойном слепом плацебо-контролируемом РКИ ASCOMALVA (Effect of association between a cholinesterase inhibitor and GPC on cognitive deficitsin Alzheimer’s disease associated with cerebrovascular injury), участниками которого были пациенты с БА и сопутствующим ишемическим поражением церебральных сосудов, показано, что комбинация ХАФ с иХЭ донепезилом превосходит монотерапию донепезилом по большинству тестов и хорошо переносится больными [41]. В нескольких российских исследованиях были получены хорошие результаты при применении комбинации ХАФ с этилметилгидроксипиридина сукцинатом (ЭМГПС) у больных с нарушениями мозгового кровообращения [42–47].
ЭМГПС – отечественный препарат из группы производных 3-оксипиридинов, обладающий комплексным механизмом действия, позволяющим ему реализовывать свои эффекты на трех уровнях – нейрональном, сосудистом и метаболическом, и оказывать благоприятное влияние не только на ЦНС, но и на периферические органы и ткани [45]. Препарат способен ингибировать процессы свободно-радикального окисления и подавлять окислительный стресс, который рассматривается в качестве одного из наиболее значимых факторов патогенеза нейродегенеративных заболеваний, в т. ч. БА и других видов деменции, болезни Паркинсона, эпилепсии, рассеянного склероза, бокового амиотрофического склероза. ЭМГПС корригирует нарушенные при старении процессы обучения и памяти, способствует улучшению процессов сохранения и воспроизведения информации, снижает уровни маркеров старения (липофусцина, малонового альдегида, холестерина) в головном мозге и крови, уменьшает проявления неврологического дефицита и восстанавливает эмоциональный и вегетативный статус пациентов пожилого возраста [46].
Кроме того, он оказывает благоприятные эффекты на сердечно-сосудистую и свертывающую систему крови: препятствует активации перекисного окисления липидов, снижает гиперлипидемию и содержание атерогенных липопротеидов и триглицеридов, повышает уровень липопротеидов высокой плотности в сыворотке крови, тормозит локальные сосудистые механизмы атерогенеза и уменьшает риск развития патологических изменений в сосудистой стенке. Одновременно ЭМГПС улучшает микроциркуляцию и реологические свойства крови путем угнетения образования тромбоксана А и усиления продукции простациклина [46].
Вышеперечисленные свойства позволяют рассматривать ЭМГПС в качестве препарата для базовой терапии цереброваскулярных заболеваний. Его эффективность продемонстрирована при применении в качестве терапевтического и профилактического средства при острых нарушениях мозгового кровообращения, дисциркуляторной энцефалопатии, вегетососудистой дистонии, атеросклеротических нарушениях функций мозга и при других состояниях, сопровождающихся гипоксией тканей [47].
Механизмы действия и фармакологические свойства ХАФ и ЭМГПС дополняют друг друга с точки зрения влияния как на когнитивные функции, так и на соматические симптомы. Комплексное применение ХАФ и ЭМГПС позволяет обеспечить процессы нейропротекции и нейропластичности клеток мозга необходимой энергией, а синергизм между компонентами комбинации, обусловленный их действием на разные этапы патогенеза, способствует усилению терапевтического эффекта и сокращению длительности лечения, что подтверждается результатами клинических исследований данной комбинации.
Так, синергидный эффект между компонентами комбинации был продемонстрирован при применении Церетона (ХАФ) и Нейрокса (ЭМГПС) в исследовании с участием 49 пациентов в возрасте от 60 до 85 лет с впервые диагностированным ишемическим инсультом и повторным нарушением мозгового кровообращения, большинство из которых страдали артериальной гипертензией, сердечными аритмиями и нарушениями обмена глюкозы [42]. Церетон вводили внутривенно в суточной дозе 1000 мг; Нейрокс – внутривенно капельно (250 мг/5,0 мл в 250 мл физраствора). Длительность лечения составила 14 дней, период наблюдения – 30 дней. Применение комбинации ассоциировалось с положительной динамикой в восстановлении сознания и регрессе очаговых неврологических симптомов. Наряду с высокой эффективностью отмечена ее хорошая переносимость больными пожилого и старческого возраста. Аналогичные данные были получены при применении комбинации ХАФ и ЭМГПС в другом исследовании у пациентов с тяжелым ишемическим инсультом [43]. Применение этой комбинации рекомендуют и в комплексной терапии других цереброваскулярных заболеваний [44–47].
Таким образом, ХАФ представляется эффективным и безопасным препаратом при когнитивных расстройствах различного генеза, а его комбинация с ЭМГПС способствует усилению терапевтического эффекта и сокращению длительности лечения у больных с цереброваскулярными заболеваниями.
Литература
1. Захаров В.В. Диагностика и лечение умеренных когнитивных нарушений // Неврология, нейропсихиатрия, психосоматика. 2009. Вып. № 2. С. 14–19.
2. Moore A., Patterson C., Lee L. et al. Fourth Canadian Consensus Conference on the Diagnosis and Treatment of Dementia: recommendations for family physicians // Can. Fam. Physician. 2014. Vol. 60. № 5. P. 433–438.
3. Деменции: руководство для врачей / Н.Н. Яхно и др. МЕДпресс-информ, 2010. 264 с.
4. Lobo A., Launer L.J., Fratiglioni L., et al. Prevalence of dementia and major subtypes in Europe: A collaborative study of population-based cohorts. Neurologic Diseases in the Elderly Research Group // Neurol. 2000. Vol. 54. № 11 (Suppl. 5). S4–9.
5. Hugo J., Ganguli M. Dementia and Cognitive Impairment: Epidemiology, Diagnosis, and Treatment // Clin. Geriatr. Med. 2014.Vol. 30. № 3. P. 421–442.
6. Mayo M.C., Bordelon Y. Dementia with lewy bodies // Semin. Neurol. 2014. Vol. 34. № 2. P. 182–188.
7. Ramanan V.K., Saykin A.J. Pathways to neurodegeneration: mechanistic insights from GWAS in Alzheimer’s disease, Parkinson’s disease, and related disorders // Am. J. Neurodegener. Dis. 2013. Vol. 2. № 3. P. 145–175.
8. Russ T.C., Morling J.R. Cholinesterase inhibitors for mild cognitive impairment // Cochrane Database Syst. Rev. 2012. Vol. 9. CD009132.
9. Wang H.F., Yu J.T., Tang S.W. et al. Efficacy and safety of cholinesterase inhibitors and memantine in cognitive impairment in Parkinson’s disease, Parkinson’s disease dementia, and dementia with Lewy bodies: systematic review with meta-analysis and trial sequential analysis // J. Neurol. Neurosurg. Psychiatry. 2014. May 14.
10. McKeith I., Mintzer J., Aarsland D. et al. Dementia with Lewy bodies // Lancet Neurol. 2004. Vol. 3. № 1. P. 19–28.
11. Craig D., Birks J. Galantamine for vascular cognitive impairment // Cochrane Database Syst. Rev. 2006. CD004746.
12. Craig D., Birks J. Rivastigmine for vascular cognitive impairment // Cochrane Database Syst. Rev. 2005. CD004744.
13. Hugo, Mendez M.F., Shapira J.S., McMurtray A. et al. Preliminary findings: behavioral worsening on donepezil in patients with frontotemporal dementia // Am. J. Geriatr. Psychiatry. 2007. Vol. 15. № 1. P. 84–87.
14. Press D., Alexander M. Cholinesterase inhibitors in the treatment of dementia. In: Basow DS, editor. UpToDate. Waltham (MA): UpToDate. Available at: http://www. uptodate.com/contents/cholinesterase-inhibitors-in-the-treatment-of-dementi.2013
15. Pariente A., Sanctussy D.J., Miremont-Salame G. et al. //Factors associated with serious adverse reactions to cholinesterase inhibitors: a study of spontaneous reporting // CNS Drugs. 2010. Vol. 24. № 1. P. 55–63.
16. Robinson D., Keating G. Memantine: a review of its use in Alzheimer’s disease // Drugs. 2006. Vol. 66. № 11. P. 1515–1534.
17. McKeage K. Memantine: a review of its use in moderate to severe Alzheimer’s disease // CNS Drugs. 2009. Vol. 23. P. 881–897.
18. McShane R., Areosa S.A., Minakaran N. Memantine for dementia // Cochrane Database Syst. Rev. 2006. CD003154.
19. Huey E.D., Putnam K.T., Grafman J. A systematic review of neurotransmitter deficits and treatments in frontotemporal dementia // Neurol. 2006. Vol. 66. № 1. P. 17–22.
20. Flicker L., Grimley E.J. Piracetam for dementia or cognitive impairment // Cochrane Database Syst. Rev. 2004. CD001011.
21. Jansen S.L., Forbes D., Duncan V. et al. Melatonin for the treatment of dementia // Cochrane Database Syst. Rev. 2006.CD003802.
22. Malouf R., Grimley E.J. Vitamin B6 for cognition // Cochrane Database Syst. Rev. 2003. CD004393.
23. Malouf R., Areosa S.A. Vitamin B12 for cognition // Cochrane Database Syst. Rev. 2003. CD004394.
24. Malouf R., Grimley E.J. Folic acid with or without vitamin B12 for the prevention and treatment of healthy elderly and demented people // Cochrane Database Syst. Rev. 2008. CD004514.
25. Preventing Alzheimer’s Disease and Cognitive Decline. NIH State-of-the-Science Conference April 26–28, 2010. Bethesda, Maryland Final Panel Statement.
26. FDA Drug Safety Communication: Important safety label changes to cholesterol-lowering statin drugs http://www.fda.gov/Drugs/DrugSafety/ucm293101.htm
27. Richardson K., Schoen M., French B. et al. Statins and cognitive function: a systematic review //Ann. Intern. Med. 2013. Vol. 159. № 10. P. 688–697.
28. Alzheimer?s Association. Alzheimer’s Association Trial Match . http://www.alz.org/research/clinical_trials/find_clinical_trials_trialmatch.asp.
29. Traini E., Bramanti V., Amenta F. Choline alphoscerate (alpha-glyceryl-phosphoryl-choline) an old choline-containing phospholipid with a still interesting profile as cognition enhancing agent // Curr. Alzheimer Res. 2013.Vol. 10. № 10. P.1070–1079.
30. Scapicchio P.L. Revisiting choline alphoscerate profile: a new, perspective, role in dementia? // Int. J. Neurosci. 2013. Vol.123. № 7. P. 444–449.
31. Tayebati S.K., Amenta F. Choline-containing phospholipids: relevance to brain functional pathways // Clin. Chem. Lab. Med. 2013. Vol. 51. № 3. P. 513–521.
32. Parnetti L., Mignini F., Tomassoni D. et al. Cholinergic precursors in the treatment of cognitive impairment of vascular origin: ineffective approaches or need for re-evaluation? // J. Neurol. Sci. 2007. Vol. 257. P. 264–269.
33. Barbagallo Sangiorgi G., Barbagallo M., Giordano M. et al. Alpha-glycerophosphocholine in the mental recovery of cerebral ischemic attacks. An Italian multicenter clinical trial // Ann. NY Acad Sci. 1994. Vol. 717. P. 253–269.
34. Стулин И.Д., Мусин Р.С., Солонский Д.С. Эффективность холина альфосцерата (церетон) у больных с хронической ишемией мозга // Журн. неврол и психиатр. им. С.С. Корсакова. 2009. № 7. С. 87–89.
35. Исмагилов М.Ф., Василевская О.В., Гайфутдинов Р.Т. и др. Оценка эффективности церетона в остром периоде ишемического инсульта // Журн. неврол. и психиатр. им. С.С. Корсакова. 2009. № 3. С. 35–36.
36. Буйлова Т.В., Глотова М.Е., Халак М.Е., Вашкевич В.В. Опыт применения Церетона в процессе реабилитации больных с геморрагическим инсультом // Журн. неврол. и психиатр. им. С.С. Корсакова. 2009. № 5. Вып. 2. С. 58–62.
37. Камчатнов П.Р., Абусуева Б.А., Евзельман М.А.и др. Эффективность церетона при остром ишемическом инсульте (результаты исследования СОЛНЦЕ) // Журн. неврол. и психиатр. им. С.С. Корсакова. 2012. № 3. Вып. 2. С. 10–14.
38. Левин О.С., Батукаева Л.А., Аникина М.А., Юнищенко Н.А. Эффективность и безопасность холина альфосцерата (церетона) у пациентов с болезнью Паркинсона с когнитивными нарушениями // Журн. неврол. и психиатр. им. С. С. Корсакова. 2009. Т. 109. № 11. С. 42–46.
39. Mandat T., Wilk A., Manowiec R. et al. Preliminary evaluation of risk and effectiveness of early choline alphoscerate treatment in craniocerebral injury // Neurol. Neurochir. Pol. 2003. Vol. 37. № 6. P. 1231–1238.
40. Parnetti L., Abate G., Bartorelli L. et al. Multicentre study of l-alpha-glyceryl-phosphorylcholine vs. ST200 among patients with probable senile dementia of Alzheimer’s type // Drugs Aging. 1993. Vol. 3. Р.159–164.
41. Amenta F., Carotenuto A., Fasanaro A.M. et al. The ASCOMALVA trial: association between the cholinesterase inhibitor donepezil and the cholinergic precursor choline alphoscerate in Alzheimer’s disease with cerebrovascular injury: interim results // J. Neurol. Sci. 2012. Vol. 322. P. 96–101.
42. Шмырев В.И., Крыжановский С.М. Комбинированная терапия ишемического инсульта холина альфосцератом и этилметилгидроксипиридина сукцинатом // Фарматека. 2013. № 9. С. 79–83.
43. Серегин В.И. Применение глиатилина и мексидола в интенсивной терапии тяжелого острого ишемического инсульта // Фарматека. 2006. № 5.
44. Меньщикова Е.Б. и др. Окислительный стресс: патологические состояния и заболевания. Новосибирск: Изд-во АРТА, 2008.
45. Бадалян О.Л., Савенков А.А., Таншева К.Х., Тертышник О.Ю. Возможности применения нейрокса в комплексном лечении хронической ишемии мозга // РМЖ. 2010. Т. 18. № 8. С. 455–459.
46. Бадалян О.Л., Погосян А.С., Савенков А.А. и др. Применение препаратов Нейрокс и Церетон в комплексном лечении цереброваскулярных заболеваний // РМЖ. 2011. № 12. С. 764–767.
47. Никифоров А.С. и др. Клиническая неврология. М.: Медицина, 2002. 704 с.
www.rmj.ru
Иллюзии мозга. Когнитивные искажения из-за переизбытка информации / Habr
Список в Википедии насчитывает 175 когнитивных искажений. Конечно, это далеко не полный перечень тех способов, какими наш мозг обманывает сам себя. Такой обман совсем несложен, ведь значительная часть психических процессов у человека происходит без отображения в сознании. Таким образом, становится возможным обращаться напрямую к этим основным процессам, не задевая сознательную часть.
В работе с широкими массами профессионалы используют способы обхода механизма цензуры, который в мозге фильтрует информацию, поступающего из внешнего мира. Например, если усилить информацию эмоционально, то вербальное или невербальное послание легче пройдёт встроенные фильтры сознания и надолго сохранится в памяти потребителя информации.
Большой список когнитивных искажений в Википедии классифицирован довольно расплывчато. Там представлены четыре тематические группы:
- Искажения, связанные с поведением и принятием решений.
- Искажения, связанные с вероятностями и стереотипами.
- Социально обусловленные искажения.
- Искажения, связанные с ошибками памяти.
Такая классификация не даёт возможности ясно представлять причины этих искажений. То есть из классификации не совсем понятно, с помощью каких методов можно эксплуатировать различные когнитивные искажения, почему они возникают. К тому же, многие искажения дублируются в списке под разными названиями.
Есть другой способ классификации искажений, если более конкретно ориентироваться на причину сбоя в мышлении, который обуславливает некорректное восприятие реальности. Если классифицировать их таким образом (по причине), то искажения тоже можно разделить на четыре группы, но теперь они становятся более логичными и понятными.
Четыре проблемы, из-за которых возникают когнитивные искажения:
- Слишком много информации.
- Недостаточно смысла (многозначность).
- Необходимость действовать быстро.
- Фильтрация информации для запоминания: мозг всегда предпочитает запомнить более простую и чёткую концепцию, а не сложную и двусмысленную. Даже если вторая концепция корректнее и объективнее.
Пожалуй, особенный интерес вызывает первая группа искажений, связанных с переизбытком информации. Тем более, что остальные группы концептуально связаны с ней. Создаётся впечатление, что мгновенная фильтрация, цензура и отбор информации для запоминания — основная проблема, с которой мы сталкиваемся в современную эпоху, когда количество информации слишком велико. Из-за этого возникает, наверное, бóльшая часть когнитивных искажений и некорректного восприятия окружающей реальности.
Первую группу можно поделить на пять подгрупп.
1. Мы замечаем вещи, которые уже укрепились в памяти или часто повторяются. Это многочисленная группа искажений, которую часто эксплуатируют на телевидении. Многократное повторение одного и того же практически гарантирует, что человек упустит из внимания деталь, которая упоминается мимоходом лишь однажды. Кроме того, многократное повторение лжи увеличивает вероятность, что в неё поверят.
Примеры:
- Эвристика доступности — оценка как более вероятного того, что более доступно в памяти.
- Систематическая ошибка внимания — зависимость человеческого восприятия от повторяющихся мыслей. Если постоянно думать на одну тему, то чаще обращаешь внимание на новости на эту тему.
- Эффект иллюзии правды — тенденция верить, что информация правдива, если мы слышали её много раз.
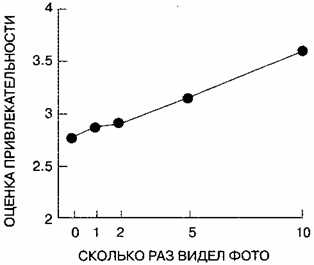
- Эффект знакомства с объектом — тенденция людей выражать необоснованную симпатию к некому объекту только потому, что они знакомы с ним.
- Забывание без контекста — затруднение вспомнить информацию в отсутствие контекста (связанных воспоминаний). И наоборот, встреча с подсказкой сразу тянет за собой всю цепочку воспоминаний. Например, если вы были в отпуске и встретили там редкий автомобиль, то встреча с таким автомобилем спустя много лет вытянет из памяти цепочку «забытых» воспоминаний об отпуске. Эффект работает также на эмоциональном уровне: некоторую информацию легче вытянуть из памяти, если вызвать «якорные» эмоции, которые контекстуально связаны с этой информацией.
- Иллюзия частоты, также известная как феномен Баадера-Майнхофа, — сразу после того, как человек узнал о какой-то новой вещи или идее, она, как ему кажется, начинает появляться повсюду. Происходит из-за того, что после того, как человек узнал о чем-то новом, его сознание начинает следить за упоминаниями, в результате чего вы замечаете это везде, где оно есть. Каждое появление вещи лишь закрепляет уверенность сознания в том, что она стала появляться повсюду.
- Разрыв эмпатии — феномен, когда человек недооценивает влияние висцеральных факторов на своё поведение. Эти факторы включают голод, жажду, сексуальное влечение, тягу к наркотику (алкоголю), физическую боль и сильные эмоции. Со стороны кажется, что человек действует импульсивно, нерационально, вышел из-под контроля. Сам человек может находить «рациональное» объяснение своим поступкам, игнорируя истинную подсознательную их причину.
- Недооценка бездействия — склонность людей недооценивать последствия бездействия в сравнении с действием с аналогичным результатом. Примером такого феномена является антивакцинаторство, когда родители предпочитают риск получить осложнения от болезни риску получить осложнения прививки, хотя риск заболеть гораздо выше риска осложнения от прививки.
- Ошибка базового процента — человек игнорирует общую частоту события и фокусируется на специфической информации. Пример: алкотестеры показывают ошибочное опьянение в 5% случаев, но ложно-отрицательных срабатываний не бывает. Полицейский останавливает водителя и проверяет его алкотестером. Прибор показывает, что водитель пьян. Вопрос: какова примерно вероятность, что водитель действительно пьян?
2. Люди склонны замечать и запоминать скорее особенные, причудливые и смешные образы, чем непричудливые или несмешные. Другими словами, мозг преувеличивает важность необычной или удивительной информации. С другой стороны, мы склонны пропускать мимо сознания информацию, которая кажется заурядной или ожидаемой.
Примеры:
- Эффект Ресторфф (эффект изоляции) — в ряду похожих объектов легче запоминается тот, который выделяется среди других. Например, число легче запоминается в ряду букв (вцу5кеквр), а не в ряду других чисел (35856896).
- Эффект превосходства картинки — картинки легче запоминаются, чем слова. Эффект подтверждён многочисленными научными экспериментами.
- Эффект самореференции — склонность людей кодировать в памяти информацию в памяти различным образом в зависимости от того, насколько она затрагивает человека лично. Эффект самореференции исследован в научной работе «Self-reference and the encoding of personal information» (Journal of Personality and Social Psychology, Vol 35(9), Sep 1977, 677-688). Специалисты по когнитивной нейробиологии определили конкретные области в префронтальной коре головного мозга, срединных структурах и теменной доле, которые задействуются, если человек считает, что информация затрагивает его лично. Эффект самореференции имеет многочисленные проявления. Например, человек гораздо лучше запоминает информацию, если она касается его лично. В рекламе человек лучше воспринимает информацию, если её рекламируют люди, похожие на него. Человек лучше запоминает дни рождения, которые близки по времени к его собственному дню рождения. Стройные женщины лучше полных женщин воспринимают образы других стройных женщин и моделей (см. научную работу «Self-referencing and consumer evaluations of larger-sized female models: A weight locus of control perspective». Marketing Letters. 18 (3): 197–209. doi:10.1007/s11002-007-9014-1).
- Уклон к негативу — вещи негативной природы даже при условии равной силы воспринимаются человеком сильнее, чем вещи положительной природы. Это относится к мыслям, эмоциям, социальным взаимоотношениям, болезненным/травмирующим событиям и т.д. Поэтому аудитория телевизионных новостей обращает больше внимания на негативные новости, а не на положительные события. Негатив воспринимается ярче, более чётко и хорошо запоминается. Эффект проявляется и в восприятии других людей: одна «негативная» характеристика человека способна перечеркнуть в восприятии множество его положительных черт. Таким образом, человек вообще без положительных черт (например, только что появившийся безликий политик) имеет преимущество перед конкурентами, у которого много положительных черт и одна отрицательная (то есть практически перед любым другим политиком). В принятии решений и управлении это когнитивное искажение очень сильно влияет на поведение человека. Бизнесмены склонны минимизировать прибыль, лишь бы гарантировать отсутствие убытков. Любой краткосрочный убыток воспринимается крайне эмоционально, даже если он объективно не влияет на общую месячную/годовую прибыль. Например, на фондовом рынке люди готовы значительно увеличить риски и продолжить инвестиции в падающую бумагу, чтобы усреднить позицию и выйти из убытка, хотя рациональным поведением было бы просто зафиксировать убыток и выйти из бумаги. Это нерациональное желание «отыграться». Любопытно, что некоторые научные исследования показывают, что данное когнитивное искажение исчезает с возрастом. Более того, у людей в зрелом возрасте иногда наблюдается даже противоположное когнитивное искажение — уклон к позитиву. То есть отрицательную информацию пожилые люди воспринимают как само собой разумеющееся и не реагируют на неё, а вот положительную информацию воспринимают сильнее (см. «The negativity bias is eliminated in older adults: Age-related reduction in event-related brain potentials associated with evaluative categorization». Psychology and Aging. 21 (4): 815–820. doi:10.1037/0882-7974.21.4.815).
3. Люди склонны замечать изменения. При этом мозг некорректно оценивает ценность новой информации в контексте направления изменения (положительное/отрицательное), а не объективно переоценивая новую информацию независимо от предыдущей.
Примеры:
- Эффект привязки — когнитивное искажение оценки числовых значений со смещением в сторону начального приближения. Эффект используют торговые сети, указывая цену нескольких штук изделия даже в отсутвие скидки за количество. Или интернет-сайты, которые предлагают пожертвовать произвольную сумму, но при этом приводят пример более крупного пожертвования. Как показали исследования, «привязав» людей к примеру крупного пожертвования, средняя сумма произвольных пожертвований оказывается выше, чем без привязки.
- Денежная иллюзия — склонность людей воспринимать номинальную стоимость денег, а не их реальную стоимость. Когнитивное искажение выражается в том, что люди не в полной мере осознают, как меняется реальная стоимость денег каждый день. Из-за этого они неадекватно воспринимают действительность, в том числе изменение номинальных цен на товары, инфляцию. Например, многие не понимают, что при изменении курса доллара к рублю их зарплата реально снизилась де-факто при сохранении её номинального значения в рублях. Власти могут поощрять это когнитивное искажение у граждан заявлениями вроде «Не нужно следить за курсом доллара» и т.д.
- Эффект фрейминга — феномен разной реакции на одинаковый выбор, в зависимости от того, как он преподносится: как положительный или отрицательный выбор. Стакан может быть наполовину пуст или наполовину полон. Выбор одинаковый, но воспринимается по-разному. Например, штрафы за опоздания действуют на людей эффективнее, чем премия за своевременные действия (очевидно, здесь действует также когнитивное искажение «уклон к негативу»). Исследование в судебной системе показало, что подсудимые чаще дают признательные показания, если те преподносятся как первый шаг к последующему освобождению после отсидки, а не как последний шаг в вольной жизни перед началом тюремного заключения.
- Закон Вебера-Фехнера — эмпирический психофизиологический закон, заключающийся в том, что интенсивность ощущения чего-либо прямо пропорциональна логарифму интенсивности раздражителя. Например, люстра, в которой восемь лампочек, ошибочно кажется настолько же ярче люстры из четырёх лампочек, насколько люстра из четырёх лампочек ярче люстры из двух лампочек.
- Консерватизм (в психологическом смысле) — когнитивное искажение новой информации, если она противоречит устоявшимся убеждениям человека.
Собственно, когнитивное искажение «консерватизм» (в психологии) можно выделить в целую отдельную категорию.
4. Людей притягивает информация, которая подтверждает их убеждения. Это действительно большая и важная категория. Она тоже связана со способом фильтровать новые данные. Если информации вокруг очень много, то человек выбирает в основном ту, которая подтверждает его мнение.
Примеры:
5. Люди склонны лучше замечать ошибки у других, чем у себя. Даже взять этот список когнитивных искажений. Кажется, что искажения восприятия скорее присутствуют у окружающих, а не у вас лично.
Примеры:
- Предубеждение слепого пятна — распознавание искажений восприятия у других людей, а не у себя. Хорошо исследовано в научных работах Эмили Пронин.
- Наивный цинизм — когнитивное искажение, форма психологического эгоизма, когда человек наивно ожидает более эгоистического поведения от других, чем есть на самом деле. Цепочка рассуждений наивного цинизма выглядит следующим образом: «У меня нет предубеждений — Если ты не согласен со мной, то у тебя предубеждения. — Твои намерения/действия отражают твои эгоистические предубеждения». Наивный цинизм противостоит противоположному когнитивному искажению — наивному реализму.
- Наивный реализм — склонность человека верить в то, что мы объективно видим окружающий мир таким, какой он есть. Несогласные с этим люди воспринимаются как неинформированные, нерациональные или во власти предубеждений. Согласно наивному научному реализму, теория, которую признало научное сообщество, обладает абсолютной истинностью, то есть даёт полный и точный образ описываемой системы объектов.
Такая классификация когнитивных искажений, связанных с переизбытком информации кажется более логичной, чем в Википедии. По крайней мере, сразу видны основные причины искажений. Хотя эта классификация всё равно остаётся довольно условной, ведь многие искажения в сознании объясняются не одной, а сразу несколькими причинами.
habr.com
Когнитивные нарушения, обусловленные критическими состояниями
У пациентов, перенесших критическое состояние, часто отмечается снижение активности мыслительных функций различной выраженности и продолжительности. С учетом растущего количества тяжелых больных, поступающих в отделения и палаты интенсивной терапии, долгосрочное ухудшение мыслительных процессов может стать значительной проблемой для общественного здравоохранения, оказывая существенное негативное влияние на качество жизни пациента после перенесенного критического состояния.
Впервые когнитивные нарушения у больных, перенесших критическое состояние, были отмечены в кардиохирургии и расценивались изначально как следствие перенесенной интраоперационно гипоксии, в связи с чем П. Бэдфордом в 1955 г. Была сформулирована концепция послеоперационных когнитивных дисфункций (ПОКД).
В 80–90-х годах прошлого века появились публикации, в которых отмечалось, что когнитивные нарушения могут наблюдаться у кардиологических больных еще до операции. Было отмечено, что послеоперационные когнитивные дисфункции могут развиваться у больных и при некардиохирургических операциях.
В начале XXI века проблема когнитивных нарушений как в послеоперационном периоде, так и при других критических состояниях приобрела значительную актуальность, однако, несмотря на это и на почти шестидесятилетнюю историю изучения послеоперационных когнитивных дисфункций, в мире до сих пор нет консенсуса относительно как определения самой этой патологии, так и набора диагностических тестов, применяемых для оценки состояния когнитивных функций.
Когнитивные функции являются наиболее сложно организованными, поскольку они обеспечивают адаптацию человека не только к физическим условиям среды обитания, но и к существованию в конкретной социальной среде.
Отличие когнитивных функций как механизма адаптации к условиям жизни от других механизмов заключается в том, что они позволяют прогнозировать еще не наступившие изменения в окружающей или социальной среде и заранее формировать стратегию адаптации.
Реализация когнитивных функций требует объединенного и согласованного участия практически всех структур головного мозга. Именно поэтому малейшая дискоординация, малейшее рассогласование деятельности клеток нервной системы проявляются нарушением прежде всего этих функций.
Из этого следует, что любое, даже самое незначительное нарушение функционирования ЦНС обязательно проявляется снижением когнитивных функций в той или иной степени, а значит, изучение состояния когнитивных функций может быть использовано в качестве мониторируемого признака состояния ЦНС. Прежде всего это важно в неврологии и нейрохирургии, но не менее важным использование такого мониторирования является и для анестезиологии и интенсивной терапии.
Одной из форм острой дисфункции головного мозга, которая может быть обусловлена критическим состоянием и ассоциируется с повышенным уровнем смертности, является делирий. Кроме того, факторы, вызывающие делирий, включая использование седативных и анальгезирующих средств, также могут способствовать долгосрочной познавательной дисфункции.
Исследование когнитивных функций должно обязательно учитывать выраженность болевого фактора, поскольку в нейрональную сеть, активируемую при болевых стимулах, вовлечены не только проекционные соматосенсорные области коры больших полушарий, но и структуры головного мозга, участвующие в реализации когнитивных функций, мотиваций, эмоций.
На состояние когнитивных функций влияет не только острая по срокам развития боль, но и хроническая. По данным литературы, хроническая боль наиболее часто сопровождается нарушением отсроченного воспроизведения и памяти, связанной с вербальным материалом. Так, у пациентов с хронической болью в спине вне зависимости от возраста выявляются когнитивные расстройства, проявляющиеся в нарушении памяти, внимания, гибкости мышления и скорости обработки информации.
Можно выделить пять факторов, вызывающих редукцию функций и структуры любого органа:
- Снижение или полное отсутствие потребности в функции.
- Необеспеченность органа энергией, необходимой для выполнения функции.
- Необеспеченность органа веществами, необходимыми для реализации функции.
- Нарушение внутриклеточного гомеостаза и метаболизма в клетках органа.
- Нарушение взаимодействия между клетками внутри органа и с клетками других органов.
Критические состояния, а также методы анестезии и интенсивной терапии являются факторами, способствующими редукции когнитивных функций, поскольку у больного, находящегося в критическом состоянии, реализуются все пять причин снижения активности когнитивных функций:
- уменьшается потребность в когнитивных функциях;
- ухудшается энергетическая обеспеченность когнитивных функций;
- нарушается обеспечение веществами, необходимыми для реализации когнитивных функций,
- внутриклеточный гомеостаз,
- соотношение анаболических и катаболических процессов,
- межклеточное взаимодействие.
Снижение потребности в когнитивных функциях может носить временный и постоянный характер. Постоянное снижение потребности в когнитивных функциях может наблюдаться в пожилом возрасте или при наличии хронического заболевания, сопровождающегося стойкой или длительной инвалидизацией и невозможностью дальнейшей работы по специальности, и может быть обусловлено изменением ритма жизни, отсутствием необходимости в мыслительной деятельности прежней интенсивности, сокращением контактов на бытовом уровне, а также сенсорной недостаточностью вследствие ухудшения зрения и слуха.
Временное снижение потребности в когнитивных функциях возникает в результате госпитализации, ограничения в связи с этим круга привычного общения и привычной интеллектуальной нагрузки, из-за сосредоточенности на состоянии своего здоровья и ощущениях, связанных с болезнью.
Эта причина снижения когнитивных функций в какой-то степени может быть устранена или значительно нивелирована без применения лекарственных препаратов — достаточно обеспечить больного дозированной интеллектуальной нагрузкой, обеспечивать достоверной и доступной его восприятию информацией о методах применяемого лечения, изменениях в состоянии его здоровья и перспективах лечения.
Кроме того, временное снижение потребности в когнитивных функциях может возникнуть при дефиците сенсорной нагрузки, что наблюдается, например, в результате анестезии и проявляется в виде послеоперационной когнитивной дисфункции.
Второй фактор, вызывающий снижение когнитивных функций, — недостаточное производство энергии для их реализации — может быть проявлением различных критических состояний, сопровождающихся гипоксией нейронов коры головного мозга, токсическим угнетением мозгового метаболизма или недостаточным поступлением глюкозы в нейроны.
Кроме глюкозы и кислорода, необходимых для выработки энергии, нейроны нуждаются и в других веществах, таких, например, как вода и электролиты, дисбаланс которых в организме может вызвать серьезные нарушения в работе ЦНС.
Существенное влияние на когнитивные функции оказывает также состояние обмена медиаторов и передачи импульсов на уровне синаптической щели, что может наблюдаться как при некоторых видах острых экзогенных интоксикаций, так и при различных заболеваниях, сопровождающихся образованием эндогенных нейротоксинов.
Механизмы развития когнитивных нарушений в настоящее время недостаточно понятны, но, очевидно, включают:
- гипоксию;
- нарушение регуляции обмена глюкозы;
- расстройства метаболизма;
- воспалительные процессы;
- эффекты седативных и наркотических препаратов.
Соответственно, любые критические состояния, сопровождающиеся этими патогенетическими факторами, могут вызывать ухудшение когнитивных функций той или иной степени.
В многоцентровом проспективном когортном исследовании BRAIN-ICU, включавшем пациентов терапевтического или хирургического ОИТ, было выявлено, что каждый четвертый пациент спустя 12 месяцев после перенесенного критического состояния имел снижение когнитивных функций, по степени тяжести сопоставимое с легкой формой болезни Альцгеймера.
Помимо этого, у каждого третьего пациента когнитивный дефицит, как правило, был связан с умеренным травматическим повреждением головного мозга.
Познавательная дисфункция затрагивала больше нейропсихологических областей по сравнению с болезнью Альцгеймера, однако была схожа с нарушениями в результате травмы головного мозга умеренной степени. Только у 6 % пациентов подтвердилось наличие когнитивной дисфункции легкой или средней степени тяжести до поступления в ОИТ. Это свидетельствовало о том, что глубокие когнитивные нарушения развились у большинства пациентов впервые.
Долгосрочное когнитивное снижение имело место как у пациентов пожилого возраста, так и у более молодых, независимо от наличия коморбидных состояний в анамнезе. Нарушение когнитивных функций негативно сказывается на качестве жизни больного и его окружения.
Согласно Н.Н. Яхно, принято выделять три степени когнитивных нарушений:
- легкие;
- умеренные;
- тяжелые.
Самой тяжелой формой когнитивных нарушений является деменция. Кроме того, в последнее время выделяют такую разновидность когнитивных нарушений, как мягкое когнитивное снижение, которое еще получило название «субъективные когнитивные нарушения», долгое время, считавшееся проявлением преимущественно тревожного расстройства или вариантом нормы.
Тяжелым и когнитивными нарушениями (ТКН) называют моно- или полифункциональные расстройства когнитивных функций, которые приводят к полной или частичной утрате независимости и самостоятельности пациентом, т.е. вызывают профессиональную, социальную и/или бытовую дезадаптацию. К ТКН относится, в частности, деменция дегенеративной или сосудистой природы.
Умеренные когнитивные нарушения представляют собой моно- или полифункциональные расстройства когнитивных функций, которые выходят за рамки среднестатистической возрастной нормы, но не вызывают дезадаптацию, хотя могут приводить к трудностям в сложных и непривычных для пациента ситуациях.
Легкие когнитивные нарушения констатируют в случае снижения одной или нескольких когнитивных функций по сравнению с исходным более высоким уровнем (индивидуальной нормой). Как правило, легкие когнитивные нарушения не вызывают трудностей в быту и профессиональной деятельности.
Субъективные когнитивные нарушения являются вариантом нормы и связаны не с поражением собственно памяти, а с физиологическими колебаниями внимания. Внимание, в свою очередь, определяется рядом факторов — мотивацией, напряженностью бодрствования, количеством предъявлений запоминаемого материала, увеличением объема работы и/или снижением количества и качества отдыха.
Наличие у больного когнитивных нарушений прямо не влияет на течение критического состояния, но известно, что создание положительного настроя на лечение, активное участие и заинтересованность больного в лечебном процессе являются факторами, способствующими более быстрому и более качественному выздоровлению, а значит, мероприятия по коррекции когнитивных нарушений, обусловленных критическими состояниями, могут способствовать более быстрому восстановлению эффективного функционирования и других систем, а вместе — способствовать более быстрому купированию критического состояния.
С другой стороны, контроль состояния и динамики когнитивных функций больного, находящегося в критическом состоянии, может помочь своевременному выявлению ухудшения соматического статуса и позволит спрогнозировать дальнейшее течение критического состояния.
Таким образом, когнитивные нарушения, обусловленные критическими состояниями, представляют собой, с одной стороны, значительную проблему для анестезиологии и интенсивной терапии, поскольку могут усугублять течение острого периода, а с другой стороны, изменения состояния когнитивных функций могут помочь в раннем выявлении отрицательной динамики в течении критического состояния.
Поскольку когнитивные нарушения при критических состояниях развиваются вследствие нарушения нормального функционирования ЦНС, вполне оправданным будет считать их проявлением острой церебральной недостаточности. Такой взгляд на когнитивные нарушения, обусловленные критическим состоянием, позволит сформировать соответствующие принципы их профилактики и терапии.
Криштафор А.А.
2015 г.
www.ambu03.ru
Когнитивные нарушения — Википедия
Материал из Википедии — свободной энциклопедии
 Шкала оценки состояния когнитивных функций
Шкала оценки состояния когнитивных функцийКогнитивные нарушения — это снижение памяти, умственной работоспособности и других когнитивных функций[1] по сравнению с исходным уровнем (индивидуальной нормой)[2]. Когнитивными (познавательными) функциями называются наиболее сложные функции головного мозга, с помощью которых осуществляется процесс рационального познания мира и обеспечивается целенаправленное взаимодействие с ним: восприятие информации; обработка и анализ информации; запоминание и хранение; обмен информацией, построение и осуществление программы действий[2].
Когнитивные нарушения являются полиэтиологическими состояниями: причинами их могут быть большое количество различных по этиологии и патогенезу заболеваний (неврологических, психических и т. п. расстройств)[2].
Выделяют лёгкие, умеренные и тяжёлые когнитивные нарушения. Исторически проблемы когнитивных расстройств изучались преимущественно в рамках понятия «деменция»: термины «деменция», «слабоумие» означают наиболее тяжёлые когнитивные нарушения, приводящие к в повседневной жизни. Лишь впоследствии большое внимание стали уделять также и менее выраженным расстройствам[2].
Умеренные когнитивные нарушения (англ. mild cognitive impairment, MCI) представляют собой моно- или полифункциональные когнитивные расстройства, явно выходящие за рамки возрастной нормы, но не ограничивающие самостоятельности и независимости, то есть не вызывающие дезадаптации в повседневной жизни. Умеренные когнитивные нарушения, как правило, отражаются в жалобах индивидуума и обращают на себя внимание окружающих; могут препятствовать наиболее сложным формам интеллектуальной активности. Распространенность умеренных когнитивных нарушений среди пожилых лиц достигает, по данным исследований, 12—17%. Среди неврологических пациентов синдром умеренных когнитивных нарушений встречается в 44% случаев[3].
В соответствии с критериями МКБ-10 для постановки диагноза умеренных когнитивных расстройств необходимо наличие жалобы пациента на повышенную утомляемость при выполнении умственной работы, снижение памяти, внимания или способности к обучению, которые не достигают степени деменции, имеют в основе органическую природу и не связаны с делирием[4].
При лёгких когнитивных нарушениях показатели психометрических шкал могут оставаться в пределах среднестатистической возрастной нормы или отклоняться от неё незначительно, однако больные осознают снижение когнитивных способностей по сравнению с уровнем и выражают беспокойство по этому поводу. Лёгкие когнитивные нарушения отражаются в жалобах больного, но не обращают на себя внимания окружающих; не вызывают затруднений в повседневной жизни, даже в наиболее сложных её формах. Популяционные исследования распространённости лёгких когнитивных нарушений до настоящего времени не проводились, однако можно предположить, что их распространённость не уступает распространённости умеренных когнитивных нарушений[3].
Существует несколько десятков нозологических форм, в рамках которых развиваются когнитивные нарушения. К этим нозологическим формам относятся как первичные заболевания головного мозга, так и различные соматоневрологические и психические расстройства, отрицательно влияющие на когнитивные функции[2].
Основными причинами когнитивных нарушений могут являться[2]:
- Нейродегенеративные заболевания
- Болезнь Альцгеймера
- Деменция с тельцами Леви
- Фронто-темпоральная дегенерация (ФТД)
- Кортико-базальная дегенерация
- Болезнь Паркинсона
- Прогрессирующий надъядерный паралич
- Хорея Гентингтона
- Другие дегенеративные заболевания головного мозга
- Сосудистые заболевания головного мозга
- Инфаркт мозга «стратегической» локализации
- Мультиинфарктное состояние
- Хроническая церебральная ишемия
- Последствия геморрагического поражения головного мозга
- Сочетанное сосудистое поражение головного мозга
- Смешанные (сосудисто-дегенеративные) когнитивные нарушения
- Дисметаболические энцефалопатии
- Гипоксическая
- Печёночная
- Почечная
- Гипогликемическая
- Дистиреоидная (гипотиреоз, тиреотоксикоз)
- Дефицитарные состояния (дефицит В1, В12, фолиевой кислоты, белков)
- Промышленные и бытовые отравления
- Ятрогенные когнитивные нарушения (применение холинолитиков, барбитуратов, бензодиазепинов, нейролептиков, солей лития и др.)
- ВИЧ-ассоциированная энцефалопатия
- Губчатый энцефалит (болезнь Крейтцфельдта — Якоба)
- Прогрессирующие панэнцефалиты
- Последствия острых и подострых менингоэнцефалитов
- Прогрессивный паралич
- Рассеянный склероз
- Прогрессирующая дизимунная мультифокальная лейкоэнцефалопатия
- Нормотензивная (арезорбтивная) гидроцефалия
Обратимые нарушения[править | править код]
При большинстве хронических сосудистых и дегенеративных заболеваний мозга когнитивные расстройства носят необратимый характер, однако в случаях, когда причиной когнитивных расстройств являются системные метаболические нарушения, коррекция этих нарушений приводит к восстановлению психических функций. В таких случаях говорят об обратимых когнитивных расстройствах[2].
К обратимым когнитивным расстройствам относят дисметаболическую энцефалопатию, нарушения высших мозговых функций при нормотензивной гидроцефалии и, в некоторых случаях, при опухоли мозга; причиной обратимых нарушений могут быть также расстройства тревожно-депрессивного ряда. До 5% случаев когнитивных нарушений на стадии деменции (и, по-видимому, существенно больший процент на стадии лёгких и на стадии умеренных когнитивных расстройств) являются полностью обратимыми[2].
Поскольку когнитивные нарушения не всегда развиваются в результате первичного заболевания головного мозга, необходимо, кроме оценки неврологического статуса, общее физикальное исследование по органам и системам. Необходимыми мероприятиями являются общий анализ крови и мочи, исследование активности печёночных трансаминаз и гамма-ГТ, гормонов щитовидной железы, исследование концентрации билирубина, альбумина, креатинина и азота мочевины, при возможности — концентрации витамина В12 и фолиевой кислоты. Восстановление когнитивных функций после коррекции метаболических нарушений служит подтверждением диагноза[2].
ru.wikipedia.org
Когнитивные нарушения: лечение расстройства
Как неприятно отмечать у себя или близких людей ухудшение способности запоминать информацию, появление быстрой утомляемости, снижение интеллекта. Такие расстройства в работе головного мозга в медицине получили название «когнитивные нарушения». Однако не следует отчаиваться. Большое значение для людей с таким заболеванием играет адекватная терапия. Современная медицина способна обеспечить должное лечение и добиться стабильной ремиссии.
Статьи по темеЧто такое когнитивные нарушения
Когнитивные функции – это восприятие, сообразительность, способность знакомиться с новой информацией и запоминать ее, внимание, речь, ориентация в пространстве и времени, двигательные навыки. Со временем у человека начинают проявляться нарушения повседневного поведения из-за сбоев в работе когнитивных функций. Единичные случаи забывчивости – это еще не повод переживать, но если человек начинает регулярно забывать события, имена или названия предметов, то это может указывать на нарушения в деятельности мозга, тогда пациенту требуется помощь невролога.
Симптомы
Если нарушение когнитивных функций связано с левым полушарием головного мозга, то можно наблюдать такие внешние симптомы, как неспособность пациента писать, считать, читать, начинаются затруднения с логикой, анализом, исчезают математические способности. Правое полушарие, пораженное болезнью, будет давать пространственные нарушения, например, человек перестает ориентироваться в пространстве, уходит способность мечтать, сочинять, фантазировать, сопереживать, заниматься рисованием и другим творчеством.
Деятельность лобных долей мозга связана с восприятием запахов и звуков, с эмоциональным окрашиванием окружающего мира, она отвечает за опыт и запоминание. Если заболевание затрагивает теменные доли мозга, то пациент теряет возможность целенаправленно выполнять действия, он не различает, где право, где лево, не может писать или читать. Затылочные доли отвечают за способность видеть цветные картинки, анализировать, узнавать лица, предметы. Изменения в области мозжечка характеризуются неадекватным поведением и нарушением речи.


Легкое когнитивное расстройство
Его можно считать начальным этапом в цепочке сбоев высшей мозговой активности, которые по большей части, касаются памяти больного. Легкий вид нарушений может провоцироваться не только возрастными изменениями. Нередко причиной становится энцефалит или травма головы. Что такое когнитивное расстройство и как оно проявляется на внешнем плане? Это сильная утомляемость во время умственной деятельности, невозможность запоминать новую информацию, растерянность, затруднения с концентрацией внимания, проблемы при выполнении целенаправленных действий.
Нередко пациенту сложно понимать чужую речь или самому подбирать слова для передачи мыслей. Интересен тот факт, что это обратимый процесс. При сильных умственных нагрузках симптомы прогрессируют, а после хорошего отдыха исчезают. Однако есть необходимость посетить невролога и терапевта, которые проведут необходимые инструментальные исследования, назначат сдачу анализов.
Умеренные когнитивные нарушения
При ухудшении работы нескольких процессов, выходящих за рамки нормы возраста пациента, но не достигающих степени деменции, можно говорить об умеренном нарушении. По данным медицинской статистики, подобные симптомы могут встречаться у 20% людей возраста от 60 лет. Однако у большей части этих пациентов в последующие пять лет наступает деменция. У 30% людей наблюдается медленное прогрессирование болезни, но если за короткий промежуток времени случается расстройство сразу нескольких когнитивных функций, то необходима срочная консультация специалиста.
Тяжелая форма
Распространенность деменции наблюдается у пожилых пациентов, а провоцируется она, как правило, болезнью Альцгеймера. БА – это болезнь мозга, связанная с отмиранием ацетилхолинергических нейронов. Ее первыми признаками становятся утрата памяти, постоянная забывчивость жизненных событий. На следующей стадии прогрессирования патологических изменений начинается дезориентировка в пространстве, человек теряет способность выражать свои мысли, говорит бред, в быту становится беспомощен и может нуждаться в помощи близких.
Нередко выраженные нарушения когнитивных функций провоцирует сосудистая мозговая недостаточность, тогда память на жизненные события может оставаться хорошей, но страдает интеллект. Пациенты перестают различать и видеть схожесть между понятиями, их мышление замедляется, появляется трудность в концентрации внимания. Кроме этого, у человека наблюдается повышение мышечного тонуса, меняется походка. При таких признаках назначается нейропсихологическое обследование.


Причины
Нарушения делят на два вида: функциональные и органические. Функциональные расстройства провоцируются эмоциональным перенапряжением, стрессами, перегрузками. Они характерны для любого возраста и при устранении причин, как правило, проходят самостоятельно. Однако бывают случаи, когда врач решает применить медикаментозную терапию.
Органические нарушения провоцируются изменениями в головном мозге под воздействием какого-либо заболевания. Как правило, они наблюдаются в пожилом возрасте и отличаются устойчивым характером. Современная медицина предлагает продуктивные способы решения такой проблемы, позволяющие получить хороший результат. Можно назвать следующие причины нарушений:
- Недостаточность кровоснабжения клеток мозга. Сюда относят такие заболевания, как сердечно-сосудистая патология, инсульт, гипертония. Человек должен следить за своим артериальным давлением, поддерживать оптимальный уровень сахара и холестерина.
- Возрастная атрофия головного мозга или прогрессирующая болезнь Альцгеймера. В этом случае симптоматика болезни нарастает постепенно, в течение многих лет. Адекватное лечение поможет улучшить состояние пациента, стабилизировать симптомы на долгий срок.
- Проблемы обмена веществ.
- Алкоголизм и отравления.
- Сердечно-сосудистая недостаточность.
У детей
Практика детской невралгии показывает, что когнитивный дефицит появляется вследствие заболеваний, затрагивающих нервную систему маленького пациента. Это может быть, например, родовая травма или внутриутробная инфекция, врожденные обменные нарушения в нервной системе ребенка. Существует проблема скорой и верной диагностики, но чем быстрее специалисты выявят болезнь и начнут проведение адекватной терапии, тем лучше будет результат.
Когнитивные расстройства в пожилом и старческом возрасте
У пожилых пациентов головной мозг испытывает массу изменений, а его масса значительно уменьшается. Начинается этот процесс рано, еще в 30-40 лет, а к 80 годам степень потери нейронов может составлять до 50% от общей массы. Уцелевшие нейроны не остаются прежними, они претерпевают функциональные изменения. На внешнем плане это может проявляться в том числе в виде нарушений когнитивных функций.
Когнитивная дисфункция у пожилых людей выражается в чрезмерной раздражительности, обидчивости, ограниченности мышления, плохой памяти. Их настроение часто меняется, проявляются такие качества, как пессимизм, страх, тревога, недовольство другими людьми, возможна социально-бытовая дезадаптация. Отсутствие лечения приведет к катастрофическим нарушениям когнитивных функций.


Классификация
Современная классификация когнитивных расстройств основывается на степени их выраженности и делится на легкие, средние и тяжелые формы. При легких расстройствах под удар попадают такие процессы, как возможность быстро обрабатывать поступающую информацию, переключение с одного вида деятельности на другой. При умеренных расстройствах преобладает нарушение памяти, которое со временем может развиться в болезнь Альцгеймера. Тяжелые расстройства – это дезориентация во времени, страдает речь, нарушается способность воспроизведения слов, страдает психика.
Диагностика когнитивных нарушений
Она основана на субъективных жалобах самого пациента, на оценке его состояния близкими людьми и определении неврологического статуса. Кроме этого, врач проводит нейропсихологическое тестирование, назначает такие виды исследований, как компьютерная и магнитно-резонансная томография. Чтобы диагностировать наличие депрессии у пациента (она часто становится причиной развития когнитивных расстройств), применяется шкала Гамильтона.
Лечение
Когнитивное расстройство личности лечится посредством нейрометаболических лекарственных препаратов трех видов: классические средства (Пирацетам, Пиритинол, Церебролизин), препараты для лечения болезни Альцгеймера (Халина альфосцерат, Мемантин, Ипидакрин), комбинированные средства (Омарон, Циннаризин). Большой выбор нейрометаболических лекарств для регуляции когнитивных процессов делает возможным индивидуализировать лечение пациентов с нарушениями когнитивных функций.
Профилактика
Что же следует делать, чтобы избежать возникновения расстройства когнитивных функций? С юных лет необходимо заботиться о своем здоровье. Врачи рекомендуют в качестве профилактики этой проблемы ежедневно заниматься активными видами спорта, тренировать память, больше общаться. Огромную роль играет отказ от вредных привычек, достаточное употребление витаминов, правильное питание. Например, снизить риск появления расстройств поможет средиземноморская диета. В последнее время для профилактики применяются фитопрепараты из гинкго билоба.
Видео
 Нарушение когнитивных функций
Нарушение когнитивных функций
Внимание! Информация, представленная в статье, носит ознакомительный характер. Материалы статьи не призывают к самостоятельному лечению. Только квалифицированный врач может поставить диагноз и дать рекомендации по лечению, исходя из индивидуальных особенностей конкретного пациента.
Нашли в тексте ошибку? Выделите её, нажмите Ctrl + Enter и мы всё исправим! Рассказать друзьям: Комментарии для сайта Cacklesovets.net

